摘要:(3)镁条在氧气中燃烧生成氧化镁:2Mg+O2 2MgO
网址:http://m.1010jiajiao.com/timu_id_413989[举报]
(2011?静安区模拟)某化工厂联合生产纯碱、镁、阻燃剂.以白云石(CaCO3?MgCO3)为原料冶炼镁:经高温煅烧生成的氧化物在还原炉中经1200℃用硅铁还原生成镁蒸汽(铁化合价不变),镁蒸汽经冷凝为粗镁;同时以海水为原料制碱和制阻燃剂.具体流程如下:
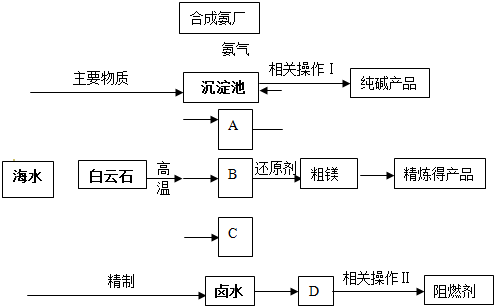
(1)分别写出A、B、C的化学式
(2)硅铁还原生成镁蒸汽时选择低压和1200℃,试分析选择这种反应条件的原因
(3)精制卤水中的MgCl2与适量石灰乳反应生成碱式氯化镁[Mg(OH)Cl]沉淀,此时溶液中主要溶质是(写化学式)
(4)描述流程中相关操作Ⅰ包括过滤、
(5)已知:Mg(OH)2(s)→MgO(s)+H2O(g)-81.5kJ;
Al(OH)3(s)→0.5Al2O3(s)+1.5H2O(g)-87.7kJ
①Mg(OH)2能起阻燃作用,其原因是
②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
(6)某化工厂利用上图所示流程联合生产纯碱、镁、阻燃剂,试分析该生产的优点
查看习题详情和答案>>

(1)分别写出A、B、C的化学式
CO2
CO2
、MgO
MgO
、CaO
CaO
;沉淀池中反应的化学方程式是CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl
CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl
.(2)硅铁还原生成镁蒸汽时选择低压和1200℃,试分析选择这种反应条件的原因
低压有利于镁蒸气的生成及分离;1200℃只有镁为气体,从速率和平衡2个角度都有利于镁的生成
低压有利于镁蒸气的生成及分离;1200℃只有镁为气体,从速率和平衡2个角度都有利于镁的生成
.(3)精制卤水中的MgCl2与适量石灰乳反应生成碱式氯化镁[Mg(OH)Cl]沉淀,此时溶液中主要溶质是(写化学式)
CaCl2
CaCl2
.(4)描述流程中相关操作Ⅰ包括过滤、
洗涤
洗涤
、煅烧(或加热)
煅烧(或加热)
.(5)已知:Mg(OH)2(s)→MgO(s)+H2O(g)-81.5kJ;
Al(OH)3(s)→0.5Al2O3(s)+1.5H2O(g)-87.7kJ
①Mg(OH)2能起阻燃作用,其原因是
Mg(OH)2受热分解时吸收大量的热使环境温度下降;同时生成的耐高温、稳定性好的MgO、覆盖在可燃物表面,产生阻燃作用
Mg(OH)2受热分解时吸收大量的热使环境温度下降;同时生成的耐高温、稳定性好的MgO、覆盖在可燃物表面,产生阻燃作用
.②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
Mg(OH)2
Mg(OH)2
.(6)某化工厂利用上图所示流程联合生产纯碱、镁、阻燃剂,试分析该生产的优点
原料易得价廉、原料利用率高、中间产物能有效地循环利用、产品结构的多样化
原料易得价廉、原料利用率高、中间产物能有效地循环利用、产品结构的多样化
.(2013?湖南模拟)资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3?yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
(3)为进一步确定实验1的产物,设计定量实验方案,如图所示:

称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:
查看习题详情和答案>>
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为
Mg(OH)2
Mg(OH)2
.猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3?yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | ①气体成分为 氢气 氢气 |
| 实验Ⅲ | ②取实验Ⅰ中的白色不溶物,洗涤,加入足量 稀盐酸 稀盐酸 |
③ 产生气泡沉淀全部溶解 产生气泡沉淀全部溶解 |
白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | ④溶液中存在 CO32- CO32- |

称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:
Mg(OH)2(CO3)2或2MgCO3?Mg(OH)2
Mg(OH)2(CO3)2或2MgCO3?Mg(OH)2
.(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:
NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2?2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行
NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2?2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行
.研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)已知石墨的标准燃烧热为y kJ?mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量.则石墨与氧气反应生成CO的热化学方程式为
(2)高温时,用CO还原MgSO4可制备高纯MgO.
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是
②由MgO可制成“镁-次氯酸盐”燃料电池,其装置示意图如图1,该电池反应的离子方程式为
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
①该反应的平衡常数表达式为K=
.
②取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的
△H
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡.
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为

查看习题详情和答案>>
(1)已知石墨的标准燃烧热为y kJ?mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量.则石墨与氧气反应生成CO的热化学方程式为
C(s)+
O2(g)=CO(g)△H=-
kJ?mol-1
| 1 |
| 2 |
| (x-0.04y) |
| 0.06 |
C(s)+
O2(g)=CO(g)△H=-
kJ?mol-1
,| 1 |
| 2 |
| (x-0.04y) |
| 0.06 |
(2)高温时,用CO还原MgSO4可制备高纯MgO.
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是
CO+2MgSO4
2MgO+CO2+SO2+SO3
| ||
CO+2MgSO4
2MgO+CO2+SO2+SO3
.
| ||
②由MgO可制成“镁-次氯酸盐”燃料电池,其装置示意图如图1,该电池反应的离子方程式为
Mg+ClO-+H2O=Cl-+Mg(OH)2
Mg+ClO-+H2O=Cl-+Mg(OH)2
.(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
①该反应的平衡常数表达式为K=
| C(CH3OH)C(H2O) |
| C(CO2)C3(H2) |
| C(CH3OH)C(H2O) |
| C(CO2)C3(H2) |
②取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的
△H
<
<
(填“>”“<”或“=”)0.③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ
>
>
KⅡ(填“>”“<”或“=”).④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡.
| 容 器 | 甲 | 乙 |
| 反应物 投入量 |
1molCO2 3molH2 |
a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
0.4<n(c)≤1mol
0.4<n(c)≤1mol
.
 镁将成为21世纪重要的轻型环保材料.
镁将成为21世纪重要的轻型环保材料.(1)海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中MgCl2
| 熟石灰 |
| 过滤 |
| 盐酸 |
| 蒸发、浓缩、结晶 |
| 脱水 |
| 通电 |
①在实验室进行过滤操作时需要用到玻璃棒,其作用是
引流
引流
.②电解熔融氯化镁的过程中,
电
电
能转化为化学
化学
能.(2)①金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧.燃烧的化学方程式为
2Mg+CO2=C+2MgO,此反应类型属于
C
C
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
②金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为-3.据此写出氮化镁的化学式
Mg3N2
Mg3N2
.(3)镁铝合金广泛用于火箭、导弹和飞机制造业等.某兴趣小组为探究镁铝合金的组成,取16g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | 5.2 | 4.0 |
1:3
1:3
.所用氢氧化钠溶液的溶质质量分数为40%
40%
.(4)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;小赵认为可能是Mg2(OH)2CO3;小花认为可能是Mg(OH)2.小赵认为小明的猜想是错误的,其理由是
氧化镁为白色固体与水缓慢反应生成氢氧化镁
氧化镁为白色固体与水缓慢反应生成氢氧化镁
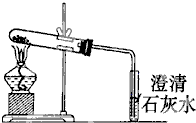
.实验探究:小赵按如图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.
实验分析:实验后,小赵认为小花的猜想也是错误的,其理由是
样品分解生成的二氧化碳使澄清石灰水变浑浊
样品分解生成的二氧化碳使澄清石灰水变浑浊
.查阅资料得出结论:Mg(OH)2 和 Mg2(OH)2CO3 都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2CO3 加热
分解的化学方程式
Mg2(OH)2CO3
2MgO+CO2↑+H2O
| ||
Mg2(OH)2CO3
2MgO+CO2↑+H2O
.
| ||