摘要:1.装置如图1―4所示
网址:http://m.1010jiajiao.com/timu_id_412496[举报]
 如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:
如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:(1)教材中是用与制O2相同的制备装置来加热制取NH3的,该反应的化学方程式为:
2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2
| ||
2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2
.
| ||
(2)下面是部分同学对于能用图1制取NH3的原因分析,有道理的是
①②③④
①②③④
.①在NH3?H2O中有平衡 NH3+H2O=NH3?H2O=NH4++OH-,NaOH使平衡向左移动; ②在NH3?H2O中有平衡阳NH3+H2O=NH3?H2O=NH4++OH-,NH4Cl 使平衡向左移动; ③NaOH 溶于水时放热,使体系的温度升高,NH3的溶解度减小;④NH4Cl与NaOH在此情况下可反应生成NH3,即NH4++OH-
| ||
(3)判断图1中烧瓶己收满NH3的现象
烧杯内的溶液变红
烧杯内的溶液变红
.(4)图2中胶头漓管中的水挤入烧瓶后,观察到的现象是
气球逐渐变大
气球逐渐变大
它说明了NH3极易溶于水
极易溶于水
.如图1是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,省略铁架台等已省略.)按下连连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…

(1)这三步操作的先后顺序依次是
(2)简要说明排空气的方法和证明空气已排尽的方法
(3)B装置所起的作用是
(4)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为
(5)若对E装置中的混合物再按图2流程实验:
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式
查看习题详情和答案>>

(1)这三步操作的先后顺序依次是
②③①
②③①
;(2)简要说明排空气的方法和证明空气已排尽的方法
打开K,使丁烷气依次流经各装置,在装置G的末端收集一小试管气体堵住管口,靠近火焰,松开手指,若没有爆鸣声,则空气排尽
打开K,使丁烷气依次流经各装置,在装置G的末端收集一小试管气体堵住管口,靠近火焰,松开手指,若没有爆鸣声,则空气排尽
;(3)B装置所起的作用是
通过观察气泡,调节K,控制气体流速
通过观察气泡,调节K,控制气体流速
;(4)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为
1:1
1:1
.(假定流经D、G装置中的气体能完全反应)(5)若对E装置中的混合物再按图2流程实验:
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ
分液
分液
Ⅱ蒸馏
蒸馏
,Na2SO3溶液的作用是(用离子方程式表示)SO32-+Br2+H2O═SO42-+2H++2Br-
SO32-+Br2+H2O═SO42-+2H++2Br-
.②已知B的碳原子数大于A的碳原子数,请写出B的结构简式
CH3-CHBr-CH2Br
CH3-CHBr-CH2Br
.如图1所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质.

(1)含酚酞的0.01mol?L-1 CH3COONa溶液显浅红色的原因为:
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01mol?L-1 CH3COONa溶液中加入少量浓盐酸,则CH3COO-水解平衡移动的方向为_
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO- )-c(Na+)=
(5)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图2,则HX的酸性
查看习题详情和答案>>

(1)含酚酞的0.01mol?L-1 CH3COONa溶液显浅红色的原因为:
CH3COO-+H2O?CH3COOH+OH-
CH3COO-+H2O?CH3COOH+OH-
(用离子方程式表示).(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是
B、D
B、D
.A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01mol?L-1 CH3COONa溶液中加入少量浓盐酸,则CH3COO-水解平衡移动的方向为_
右
右
_; 加入NaOH固体,则CH3COO-水解平衡移动的方向为左
左
(填“左”、“右”或“不移动”)(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO- )-c(Na+)=
9.9×10-7mol/L
9.9×10-7mol/L
.(填准确数值)(5)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图2,则HX的酸性
>
>
(填“>”、“=”或“<”)醋酸的酸性;稀释后,HX溶液中水电离出来的c(H+)>
>
醋酸溶液水电离出来c(H+)(填“>”、“=”或“<”).如图1所示,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.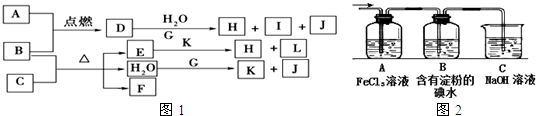
回答下列问题:
(1)K所含的化学键有
(2)D的水溶液与G反应的总离子方程式为
(3)写出工业上制取单质G的化学方程式
(4)将气体F通入如图2所示装置中写出A、B中的离子方程式:
(5)若将F通入一定量K的水溶液中,则所得溶液中各离子浓度一定满足的关系式为
查看习题详情和答案>>

回答下列问题:
(1)K所含的化学键有
离子键和共价键
离子键和共价键
.(2)D的水溶液与G反应的总离子方程式为
2Fe3++6H2O+6Na=2Fe(OH)3↓+6Na++3H2↑或2Na+2H2O═2Na++2OH-+H2↑,Fe3++3OH-=Fe(OH)3↓
2Fe3++6H2O+6Na=2Fe(OH)3↓+6Na++3H2↑或2Na+2H2O═2Na++2OH-+H2↑,Fe3++3OH-=Fe(OH)3↓
.(3)写出工业上制取单质G的化学方程式
2NaCl
2Na+Cl2↑
| ||
2NaCl
2Na+Cl2↑
.
| ||
(4)将气体F通入如图2所示装置中写出A、B中的离子方程式:
SO2+2Fe3++2H2O=SO42-+Fe2++4H+
SO2+2Fe3++2H2O=SO42-+Fe2++4H+
、SO2+I2+2H2O=4H++2I-+SO42-
SO2+I2+2H2O=4H++2I-+SO42-
.(5)若将F通入一定量K的水溶液中,则所得溶液中各离子浓度一定满足的关系式为
c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32- )
c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32- )
.
如图1是某研究性学习小组利用实验室制氯气的装置设计制取氯水并进行相关实验.
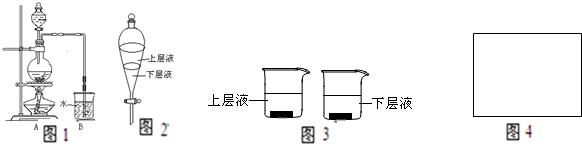
(1)A装置中发生化学反应的离子方程式为 .
(2)氯气能使湿润的红色布条褪色.对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能.请你设计实验,得出正确结论.
①提出假设假设一 .假设二 .假设三 .假设四 H2O使布条褪色
②设计实验方案
基于提出的假设,设计出实验方案(不需要作答)
③实验过程
实验①: ;实验②: .实验③:把红色布条放在水里,布条不褪色.
④得出结论 .
(3)用量筒取20mL氯水,倒入已检查完好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图2),等分层后取上层液和下层液,呈黄绿色的是 (填“上层液”或“下液”),再装入如图3所示的烧杯中,能使有色布条褪色的是 (填“上层液”或“下层液”)
(4)上述制备并吸收氯气装置的缺点是 ,如何改进 ,在图4框中画出改进的实验装置图 .
查看习题详情和答案>>

(1)A装置中发生化学反应的离子方程式为
(2)氯气能使湿润的红色布条褪色.对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能.请你设计实验,得出正确结论.
①提出假设假设一
②设计实验方案
基于提出的假设,设计出实验方案(不需要作答)
③实验过程
实验①:
④得出结论
(3)用量筒取20mL氯水,倒入已检查完好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图2),等分层后取上层液和下层液,呈黄绿色的是
(4)上述制备并吸收氯气装置的缺点是