网址:http://m.1010jiajiao.com/timu_id_4069961[举报]
| |||||||||||||||||||||||
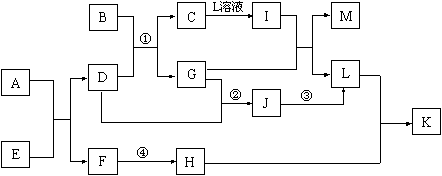
已知A—L所代表的物质(或溶液中的溶质)都是中学化学里常见的物质。通常状况下,A是淡黄色固体,D是气体单质,E是无色无味气体,K是不溶于水的酸。反应①②③是以B为原料生产化学工业重要产品的全部反应,反应④是工业生产普通玻璃的反应之一。一定条件下,各物质间的相互转化关系如下图所示(反应时加入或生成的水均没标出)。
请填写下列空白:
(1)写出下列物质的化学式:A__________;B __________;L 。
(2)画出A中金属元素的原子结构示意图_____________;指出E分子中共价键的类型(填“极性键”或“非极性键”)____________。
(3)完成下列反应方程式:
① I+G→M+L的离子方程式:____________________ ____________________。
② 写出反应④的化学方程式: ______________________ _。
CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题。
(1)上述四种气体直接排入空气中会引起酸雨的有 。
(2) 可用尿素
可用尿素 还原(尿素中C元素的化合价为+4价),反应的方程式为:
还原(尿素中C元素的化合价为+4价),反应的方程式为: 。当消耗掉12g尿素时,转移电子的物质的量是
。
。当消耗掉12g尿素时,转移电子的物质的量是
。
(3)SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的 ),改流程中发生的主要反应有:
),改流程中发生的主要反应有:

则反应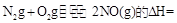 KJ/mol
KJ/mol
(4)CO可用于合成甲醇,反应方程式为 。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
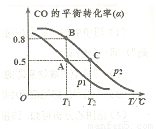
则该反应是 0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。
0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。
(5)工业上用氨水将来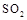 转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为
;已知25℃时,0.05mol/L(NH4)2SO4溶液的
转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为
;已知25℃时,0.05mol/L(NH4)2SO4溶液的 ,则
,则 =
(用含a的代数式表示,已知
=
(用含a的代数式表示,已知 的电离常数
的电离常数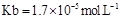 )。
)。
查看习题详情和答案>>
CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题。
(1)上述四种气体直接排入空气中会引起酸雨的有 。
(2)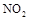 可用尿素
可用尿素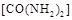 还原(尿素中C元素的化合价为+4价),反应的方程式为:
还原(尿素中C元素的化合价为+4价),反应的方程式为: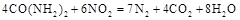 。当消耗掉12g尿素时,转移电子的物质的量是 。
。当消耗掉12g尿素时,转移电子的物质的量是 。
(3)SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的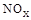 ),改流程中发生的主要反应有:
),改流程中发生的主要反应有: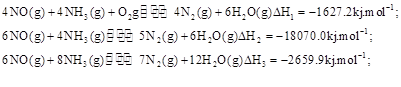
则反应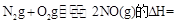 KJ/mol
KJ/mol
(4)CO可用于合成甲醇,反应方程式为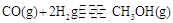 。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
则该反应是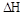 0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。
0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。
(5)工业上用氨水将来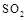 转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为 ;已知25℃时,0.05mol/L(NH4)2SO4溶液的
转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为 ;已知25℃时,0.05mol/L(NH4)2SO4溶液的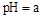 ,则
,则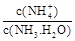 = (用含a的代数式表示,已知
= (用含a的代数式表示,已知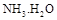 的电离常数
的电离常数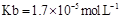 )。
)。
 (2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.
(2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.(1)上述四种气体直接排入空气中会引起酸雨的有
(2)NO2可用尿素[CO(NH2)2]还原(尿素中C元素的化合价为+4价),反应的方程式为:4CO(NH2)2+6NO2═7N2+4CO2+8H2O.当消耗掉12g尿素时,转移电子的物质的量是
(3)SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOX),改流程中发生的主要反应有:
4NO(g)+4NH3(g)+O2g?4N2(g)+6H2O(g)△H2=-18070.0kJmol-1
6NO(g)+4NH3(g)?5N2(g)+6H2O(g)△H1=-1627.2kJmol-1
6NO(g)+8NH3(g)?7N2(g)+12H2O(g)△H3=-2659.9kJmol-1
则反应N2g+O2g?2NO(g)的△H=
(5)工业上用氨水将来SO2转化成都(NH4)2SO3,再氧化成(NH4)2SO4.(NH4)2SO4溶液中离子浓度大小顺序为
c(N
| ||
| c(NH3?H2O) |
