网址:http://m.1010jiajiao.com/timu_id_406187[举报]
步骤1:呋喃的制备
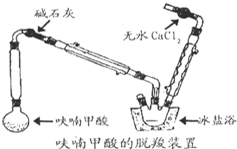
在圆底烧瓶中放置4.5g呋喃甲酸(100℃升华,呋喃甲酸在133℃熔融,230-232℃沸腾,并在此温度下脱羧),按下图安装好仪器.先大火加热使呋喃甲酸快速熔化,然后调节加热强度,并保持微沸,当呋喃甲酸脱羧反应完毕,停止加热.得无色液体呋喃(沸点:31-32℃,易溶于水).
步骤2:大环化合物八甲基四氧杂夸特烯的合成在25mL锥形瓶中加入2.7mL 95%乙醇和1.35mL浓盐酸,混匀,在冰浴中冷至5℃以下,然后将3.3mL丙酮和1.35mL呋喃的混合液迅速倒入锥形瓶中,充分混匀,冰浴冷却,静置得一黄色蜡状固体.过滤,并用3mL无水乙醇洗涤.用苯重结晶,得白色结晶八甲基四氧杂夸特烯.
(1)步骤1中用大火急速加热,其主要目的是
(2)装置图中碱石灰的作用是
(3)脱羧装置中用冰盐浴的目的是
(4)合成八甲基四氧杂夸特烯加入盐酸的目的是
(5)确论产品为八甲基四氧杂夸特烯,可通过测定沸点,还可采用的检测方法有
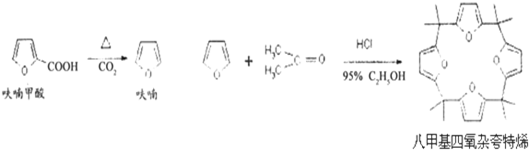
由呋哺甲酸脱羧得到呋喃与丙酮在酸性条件下缩合,可得到八甲基四氧杂夸特烯。有关实验原理及流程如下;
步骤1:呋喃的制备
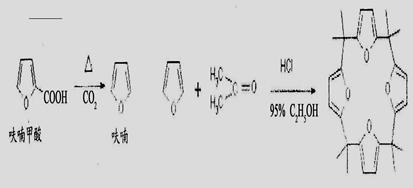
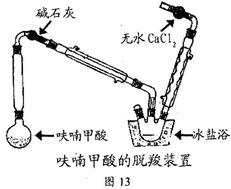
八甲基四氧杂夸特烯在圆底烧瓶中放置4.5g呋喃甲酸(100℃升华,呋喃甲酸在133℃熔融,230-232℃沸腾,并在此温度下脱羧),按图13安装好仪器。先大火加热使呋喃甲酸快速熔化,然后调节加热强度,并保持微沸,当呋喃甲酸脱羧反应完毕,停止加热。得无色液体呋喃(沸点:31-32℃,易溶于水)。
步骤2:大环化合物八甲基四氧杂夸特烯的合成在25mL锥形瓶中加入2.7mL95%乙醇和1.35mL浓盐酸,混匀,在冰浴中冷至5℃以下,然后将3.3mL丙酮和1.35mL呋喃的混合液迅速倒入锥形瓶中,充分混匀,冰浴冷却,静置得一黄色蜡状固体。过滤,并用3mL无水乙醇洗涤.用苯重结晶,得白色结晶八甲基四氧杂夸特烯。
(1)步骤1中用大火急速加热,其主要目的是 ;
(2)装置图中碱石灰的作用是 ;
(3)脱羧装置中用冰盐浴的目的是 ;无水氯化钙的作用是 ;
(4)合成八甲基四氧杂夸特烯加入盐酸的目的是 ;
(5)确论产品为八甲基四氧杂夸特烯,可通过测定沸点,还可采用的检测方法有 。
查看习题详情和答案>>
由呋哺甲酸脱羧得到呋喃与丙酮在酸性条件下缩合,可得到八甲基四氧杂夸特烯。有关实验原理及流程如下;
步骤1:呋喃的制备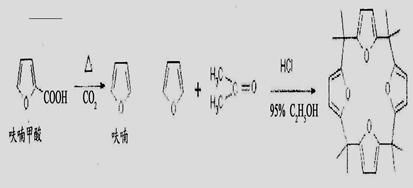
八甲基四氧杂夸特烯在圆底烧瓶中放置4.5g呋喃甲酸(100℃升华,呋喃甲酸在133℃熔融,230-232℃沸腾,并在此温度下脱羧),按图13安装好仪器。先大火加热使呋喃甲酸快速熔化,然后调节加热强度,并保持微沸,当呋喃甲酸脱羧反应完毕,停止加热。得无色液体呋喃(沸点:31-32℃,易溶于水)。
步骤2:大环化合物八甲基四氧杂夸特烯的合成在25mL锥形瓶中加入2.7mL95%乙醇和1.35mL浓盐酸,混匀,在冰浴中冷至5℃以下,然后将3.3mL丙酮和1.35mL呋喃的混合液迅速倒入锥形瓶中,充分混匀,冰浴冷却,静置得一黄色蜡状固体。过滤,并用3mL无水乙醇洗涤.用苯重结晶,得白色结晶八甲基四氧杂夸特烯。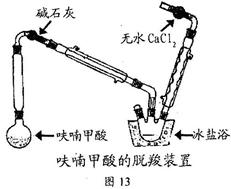
(1)步骤1中用大火急速加热,其主要目的是 ;
(2)装置图中碱石灰的作用是 ;
(3)脱羧装置中用冰盐浴的目的是 ;无水氯化钙的作用是 ;
(4)合成八甲基四氧杂夸特烯加入盐酸的目的是 ;
(5)确论产品为八甲基四氧杂夸特烯,可通过测定沸点,还可采用的检测方法有 。
下列几种情况,对中和滴定结果无影响的是
- A.向锥形瓶里的待测液中加入一定量的蒸馏水将待测液稀释
- B.滴定管尖嘴部分在滴定前有气泡
- C.盛放标准酸液的滴定管未用标准酸液润洗
- D.滴定前仰视刻度线读数,滴定后俯视刻度线读数

现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.00mL,终读数如图2所示.请回答下列问题:
(1)将样品研细后再反应,其目的是
(2)装置a的作用是
a.有利于空气中氧气充分反应b.除去空气中的水蒸气
c.有利于气体混合 d.有利于观察空气流速
(3)上述反应结束后,仍需通一段时间的空气,其目的是
(4)滴定时,标准碘溶液所耗体积为
(5)若用如图3装置替代上述实验装置d,同样可以达到实验目的是
(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有