摘要:(1)测定面粉中的水分在两只预先烘干.带盖.并精确称量好的坩埚里加入约5g面粉.盖后再精确称量.然后放入烘箱内加热到105℃.持续2-3小时.然后取出坩埚.放在干燥器中冷却.再次称量.记下质量.再次把坩埚放入烘箱.在105℃温度下加热1.5-2小时.再照上述方法冷却.称量.如果两次冷却后的质量差不超过0.01g.就能按下式算出水分的百分含量. 式中A是所取面粉样品的质量.B是干燥以后面粉的质量.面粉正常的含水量约为12%.(2)测定面粉的灰分把装有5-10g面粉的瓷坩埚放在石棉网上(加面粉前后瓷坩埚都应精确称量)加热到其中的挥发物质全部除去.再用煤气灯加强热灼烧.使坩埚中只留下黄色灰烬.再把坩埚放在干燥器中冷却.冷却后连同坩埚一起称量.求得灰烬的质量.
网址:http://m.1010jiajiao.com/timu_id_406185[举报]
下列实验中,能够达到预期目的的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 在Na2SO3溶液中加入HNO3酸化的Ba(NO3)2 ,产生白色沉淀 | 检验Na2SO3是否变质 |
| B | 将某气体通入品红溶液中,品红褪色 | 证明该气体是SO2 |
| C | 用洁净的玻璃棒蘸取NaOH溶液,点在湿润的pH试纸上,与标准比色卡对照 | 测定NaOH溶液的pH |
| D | 在两支试管中各加入4 mL 0.01 mol/L的KMnO4 酸性溶液,再分别加入0.1 mol/L H2C2O4 溶液2 mL、0.2 mol/L H2C2O4 溶液2 mL, 分别记录溶液褪色所需时间 | 探究相同条件下,溶液浓度对反应速率的影响 |
维生素C(简称VC,化学式为C6H8O6)是一种水溶性物质,其水溶液呈酸性。VC具有较强的还原性,易被空气中的氧气所氧化。在新鲜的水果、青菜和乳制品中都富含VC,如新鲜橙汁中VC的含量在500 mg·L-1左右。食物中的VC在烹调、贮存、加工时较易丢失。
(1)人体缺乏VC易得何种疾病?
(2)已知VC与I2的反应为:C6H8O6+I2=C6H6O6+2HI,碘遇淀粉变蓝。VC与I2的反应是否为氧化还原反应?氧化剂是哪种物质?
(3)针对VC的性质,你认为在炒菜和淘米的时候应该注意什么?
查看习题详情和答案>>
下列实验中,能够达到预期目的是( )
A.A
B.B
C.C
D.D
查看习题详情和答案>>
| 编号 | 实验内容 | 实验目的 |
| A | 在Na2SO3溶液中加入HNO3酸化的Ba(NO3)2,产生白色沉淀 | 检验Na2SO3是否变质 |
| B | 将某气体通入品红溶液中,品红褪色 | 证明该气体是SO2 |
| C | 用洁净的玻璃棒蘸取NaOH溶液,点在湿润的pH试纸上,与标准比色卡对照 | 测定NaOH溶液的pH |
| D | 在两支试管中各加入4mL 0.01mol/L的KMnO4酸性溶液,再分别加入0.1mol/L H2C2O4溶液2mL、0.2mol/L H2C2O4溶液2mL,分别记录溶液褪色所需时间 | 探究相同条件下,溶液浓度对反应速率的影响 |
A.A
B.B
C.C
D.D
查看习题详情和答案>>
下列实验中,能够达到预期目的是
| 编号 | 实验内容 | 实验目的 |
| A | 在Na2SO3溶液中加入HNO3酸化的Ba(NO3)2,产生白色沉淀 | 检验Na2SO3是否变质 |
| B | 将某气体通入品红溶液中,品红褪色 | 证明该气体是SO2 |
| C | 用洁净的玻璃棒蘸取NaOH溶液,点在湿润的pH试纸上,与标准比色卡对照 | 测定NaOH溶液的pH |
| D | 在两支试管中各加入4mL 0.01mol/L的KMnO4酸性溶液,再分别加入0.1mol/L H2C2O4溶液2mL、0.2mol/L H2C2O4溶液2mL,分别记录溶液褪色所需时间 | 探究相同条件下,溶液浓度对反应速率的影响 |
- A.A
- B.B
- C.C
- D.D
PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:
(一)制备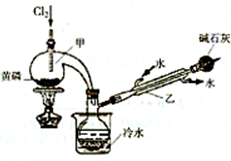
如图是实验室制备PCl3的装置(部分仪器已省略)
(1)仪器乙的名称
(2)实验室制备Cl2的离子方程式:
(3)碱石灰的作用是
(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间的CO2,其目的是
(二)提纯
粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过
(三)分析
测定产品中PCl3纯度的方法如下:迅速称取m,g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c1mol?L-lV1mL碘溶液,充分反应后再用c2mol?L-1Na2S2O3溶液滴定过量的碘,终点时消耗V2mLNa2S2O3溶液.
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应.根据上述数据,该产品中PCl3的质量分数为
×100%
×100%(用含字母的代数式表示、不必化简)
查看习题详情和答案>>
| 熔点/℃ | 沸点/℃ | 密度/g?mL | 其他 | |||||||||
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2
2P+5Cl2(过量)
| ||||||||
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 | ||||||||
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于 PCl3 |

如图是实验室制备PCl3的装置(部分仪器已省略)
(1)仪器乙的名称
冷凝管
冷凝管
;(2)实验室制备Cl2的离子方程式:
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
;
| ||
(3)碱石灰的作用是
吸收多余的氯气,防止污染环境
吸收多余的氯气,防止污染环境
,防止空气中的水分进入影响产品
防止空气中的水分进入影响产品
;(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间的CO2,其目的是
排净装置中的空气,防止空气中的水分和氧气与PCl3反应
排净装置中的空气,防止空气中的水分和氧气与PCl3反应
.(二)提纯
粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过
蒸馏
蒸馏
(填实验操作名称),即可得到PCl3的纯品.(三)分析
测定产品中PCl3纯度的方法如下:迅速称取m,g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c1mol?L-lV1mL碘溶液,充分反应后再用c2mol?L-1Na2S2O3溶液滴定过量的碘,终点时消耗V2mLNa2S2O3溶液.
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应.根据上述数据,该产品中PCl3的质量分数为
(c1V1-
| ||
| m |
(c1V1-
| ||
| m |