网址:http://m.1010jiajiao.com/timu_id_406157[举报]
[2012·合肥市第二次质检](13分)某化学兴趣小组对加碘食盐中碘酸钾进行研究,查阅资料得知:碘酸钾是一种白色粉末,常温下很稳定,加热至5600C开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、过氧化氢等物质作用,被还原为单质碘。
(1)学生甲设计实验测出加碘食盐中碘元素的含量,步骤如下:
a.称取wg加碘盐,加适量蒸馏水溶解;
b.用稀硫酸酸化,再加入过量KI溶液;
c.以淀粉为指示剂,用物质的量浓度为1.00×10-3mol/L的Na2S2O3溶液滴定(滴定时的反应方程式:(I2+2S2O32-=2 I-+2S4O62-)。
滴定时Na2S2O3溶液应放在_________ (填“酸式滴定管”或“碱式滴定管”),滴定至终点时消耗Na2S2O3溶液20. 00mL,其终点颜色变化为_________;加碘食盐样品中的碘元素含量是_________mg/kg(以含w的代数式表示)。
(2)学生乙对纯净的NaCl(不含KIO3)进行了下列实验:
|
顺序 |
步骤 |
实验现象 |
|
① |
取少量纯净的NaCl,加蒸馏水溶解 |
溶液无变化 |
|
② |
滴入淀粉KI溶液,振荡 |
溶液无变化 |
|
③ |
然后再滴加H2SO4,振荡 |
溶液变蓝色 |
请推测实验③中产生蓝色现象的可能原因:__________________;根据学生乙的实验结果,请对学生甲的实验结果作出简要评价___________________________。
(3)工业上通常用电解KI溶液的方法来制备碘酸钾,电解过程中请你帮助学生丙设计实验来判断电解是否完全。仪器不限,可选的试剂:淀粉溶液、H2O2溶液、稀硫酸。
|
实验操作 |
实验现象及结论 |
|
|
|
查看习题详情和答案>>
[2012·合肥市第二次质检](13分)某化学兴趣小组对加碘食盐中碘酸钾进行研究,查阅资料得知:碘酸钾是一种白色粉末,常温下很稳定,加热至5600C开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、过氧化氢等物质作用,被还原为单质碘。
(1)学生甲设计实验测出加碘食盐中碘元素的含量,步骤如下:
a.称取wg加碘盐,加适量蒸馏水溶解;
b.用稀硫酸酸化,再加入过量KI溶液;
c.以淀粉为指示剂,用物质的量浓度为1.00×10-3mol/L的Na2S2O3溶液滴定(滴定时的反应方程式:(I2+2S2O32-=2 I-+2S4O62-)。
滴定时Na2S2O3溶液应放在_________ (填“酸式滴定管”或“碱式滴定管”),滴定至终点时消耗Na2S2O3溶液20. 00mL,其终点颜色变化为_________;加碘食盐样品中的碘元素含量是_________mg/kg(以含w的代数式表示)。
(2)学生乙对纯净的NaCl(不含KIO3)进行了下列实验:
| 顺序 | 步骤 | 实验现象 |
| ① | 取少量纯净的NaCl,加蒸馏水溶解 | 溶液无变化 |
| ② | 滴入淀粉KI溶液,振荡 | 溶液无变化 |
| ③ | 然后再滴加H2SO4,振荡 | 溶液变蓝色 |
(3)工业上通常用电解KI溶液的方法来制备碘酸钾,电解过程中请你帮助学生丙设计实验来判断电解是否完全。仪器不限,可选的试剂:淀粉溶液、H2O2溶液、稀硫酸。
| 实验操作 | 实验现象及结论 |
| | |
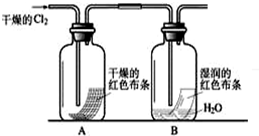
①写出Cl2与水反应的离子方程式
②通入Cl2后,从集气瓶A、B的现象可得出的结论是
(2)
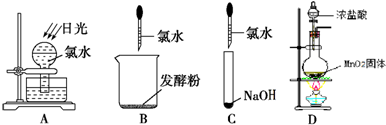
①如图所示,上述实验过程中,不会产生气体的是
②写出反应D的化学方程式
(3)碘是人体中不可缺少的微量元素,食盐中加入碘元素能有效防止缺碘引起的疾病.以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%.现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%.
①食盐中加入碘化钾的碘损失率高的原因是
②萃取碘水中的碘时,一般选用的试剂是(填字母)
A.酒精 B.四氯化碳 C.醋酸 D.硝酸银溶液
③可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾.反应的化学方程式为:5KI+KIO3+6HCl=6KCl+3I2+3H2O,反应的现象是
I.(1)配制标准溶液:称取O.30g NaNO2配成1000mL溶液A.该操作中所用到的玻璃仪器除烧杯、容量瓶外还有
(2)量取5.OO mL溶液A,稀释至1L,得溶液B.准确量取5.00mL溶液A应选用的计量仪器是
Ⅱ.配制标准色阶:取6只规格均为10mL的比色管,分别加入体积不等的溶液B,不足10mL,再加少许(约0.3g)氨基苯磺酸 (
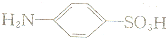 )粉末,结果如下::
)粉末,结果如下::| 色阶序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入溶液B的体积(mL | 0.0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
| 反应后溶液颜色 | 由无色变为由浅到深的樱桃红色 | |||||
(1)比色法适于
(2)若水样显色后与色阶中的6号颜色相同,表明水样中含NO2-为
(3)用NaNO2晶体直接配制溶液B的缺点是
(4)如果水样显色后比6号还深,应采取的措施是
(2)亚硝酸钠有毒,其外观和咸味与食盐很相似,因此要防止因误食亚硝酸钠而发生事故.亚硝酸钠和氯化钠的部分性质如下表:
| 性质 | 亚硝酸钠 | 氯化钠 |
| 1.酸性条件下的稳定性 | 微热时分解为NO和NO2 | 微热时不分解 |
| 2.熔点 | 271℃ | 801℃ |
| 3.室温时的溶解度 | 约80g | 约35g |
②碘是人体中不可缺少的
③食盐中加入碘元素能有效防止缺碘引起的疾病.以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%.现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%.食盐中加入碘化钾的碘损失率高的原因是
a.碘化钾被氧化,造成碘化钾的碘损失率高.
b.碘化钾升华,造成碘化钾的碘损失率高.
c.碘化钾与食物中的成分发生反应,造成碘化钾的碘损失率高.
④萃取碘水中的碘时,一般选用的试剂是(填字母)
A.酒精 B.四氯化碳 C.乙酸
⑤可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾.反应化学方程式为:5KI+KIO3+6HCl═6KCl+3I2+3H2O,反应的现象是
⑥已知碘酸钾受热易分解,你认为在用碘酸钾加碘盐进行烹饪时应注意什么问题?
(3)糖类、油脂、蛋白质都是人体必需的营养物质.
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(-NH2)和
③淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水.写出葡萄糖在体内被氧化的化学方程式:
| 酶 |
| 酶 |