网址:http://m.1010jiajiao.com/timu_id_406069[举报]
一、1.解析:设原溶液中水的质量为w g,R的质量为 m g,R的溶解度为S g,则有:

根据比例性质,可设:?

S= ×100=
×100=
答案:B?
2.解析:注意体积效应。?
答案:B?
3.解析:因H2SO4溶液的密度随浓度增大而增大,是一个变值而不是一个定值。设稀释后溶液密度为ρ′,则有:18× ×10-3=9×
×10-3=9× ×10-3,2
×10-3,2 =
= ,因为
,因为
ρ′<ρ,故V<100(mL)。
答案:A?
4.解析:NH3+2O2===HNO3+H2O?
HNO3%= ×100%=78%
×100%=78%
答案:A
5.AB 6.B 7.B 8.D 9.C?
二、10.
11.
 g
g
12.(1)G、E、C、H、F(或E、G、C、H、F)?
(2)BCD
14.(1)0.0813 mol?L-1 (2)32 mL?
15.(1)四种?
①KOH,K2CO3 ②K2CO3 ③K2CO3,KHCO3?④KHCO3?
(2)解:2KOH+CO2 === K2CO3+H2O?
22.4 138?
2.24 x=13.8?
KOH+CO2===KHCO3?
22.4 100?
2.24 x=10.0?
从上面两方程知:生成的固体全部是K2CO3时应该是 =0.100 mol
=0.100 mol
若K2CO3为a mol,则KHCO3为(0.100-a)mol?
则得方程
即K2CO3和KHCO3各为0.050 mol?
K2CO3为:
KHCO3为:
依K+守恒的要求,设KOH溶液浓度为c则:?
0.300 Lc=0.050 mol×2+0.050 mol c=0.50 mol?L-1
已知甲、乙溶质质量分数与密度的关系如下表:
溶质质量分数 | 甲溶液密度(g/cm3) | 乙溶液密度(g/cm3) |
1% | 0.95 | 1.02 |
5% | 0.92 | 1.04 |
10% | 0.90 | 1.07 |
甲物质的1%的溶液与9%的溶液等体积混合,乙物质的1%的溶液与9%的溶液等体积混合后,下列叙述正确的是
A.混合后甲、乙溶液质量分数均大于5%
B.混合后乙溶液质量分数大于5%,甲溶液质量分数小于5%
C.混合后甲溶液质量分数大于5%,乙溶液质量分数小于5%
D.混合后甲、乙溶液质量分数均等于5%
查看习题详情和答案>>|
已知甲、乙溶质的质量分数与溶液密度的关系如下表所示:
甲物质的1%的溶液与9%的溶液等体积混合,乙物质的1%的溶液与9%的溶液等体积混合,下列叙述中,正确的是 | |
| [ ] | |
A. |
混合后,甲、乙溶液中溶质的质量分数均大于5% |
B. |
混合后,乙溶液中溶质的质量分数大于5%,甲溶液中溶质的质量分数小于5% |
C. |
混合后,甲溶液中溶质的质量分数大于5%,乙溶液中溶质的质量分数小于5% |
D. |
混合后,甲、乙溶液中溶质的质量分数均等于5% |
|
已知甲、乙溶质的质量分数与溶液密度的关系如下表所示:
甲物质的1%的溶液与9%的溶液等体积混合,乙物质的1%的溶液与9%的溶液等体积混合,下列叙述中,正确的是 | |
| [ ] | |
A. |
混合后,甲、乙溶液中溶质的质量分数均大于5% |
B. |
混合后,甲溶液中溶质的质量分数大于5%,乙溶液中溶质的质量分数小于5% |
C. |
混合后,乙溶液中溶质的质量分数大于5%,甲溶液中溶质的质量分数小于5% |
D. |
混合后,甲、乙溶液中溶质的质量分数均等于5% |
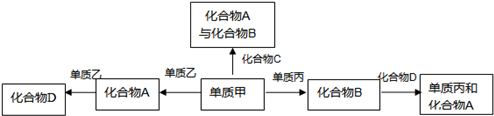
Ⅰ.(1)化合物A的电子式为______;化合物C的结构简式______.
(2)已知常温下测得1g C完全燃烧可放出15.6kJ热量,则C完全燃烧的热化学方程式可表示为:______.
(3)下列说法正确的是______.
A、上述所涉及的化合物中有两种是电解质 B、图中五个转化关系,有三个是化合反应
C、上述所涉及的化合物的晶体均是分子晶体 D、图中五个转化关系均为氧化还原反应
(4)用甲、丙、乙、硫酸溶液可以构成一原电池,则电极材料可以为______,正极的电极反应式为______.
Ⅱ.向某密闭容器中加入 0.4mol B、0.3mol D和一定量的A三种气体.一定条件下发生反应,各物质浓度随时间的变化如下图中甲图所示.乙图为 t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同条件,所用条件均不同.已知t3~t4阶段为使用催化剂[已知 t0~t1阶段 c ( A)未画出].
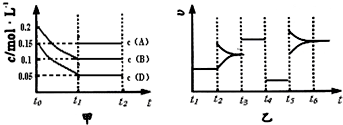
(1)A的起始物质的量为______;
(2)此条件下的化学平衡常数为______;
(3)t4~t5阶段改变的条件为______.
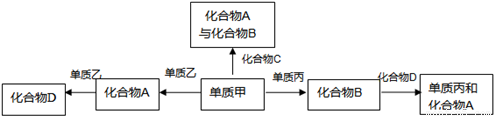
Ⅰ.(1)化合物A的电子式为______;化合物C的结构简式______.
(2)已知常温下测得1g C完全燃烧可放出15.6kJ热量,则C完全燃烧的热化学方程式可表示为:______.
(3)下列说法正确的是______.
A、上述所涉及的化合物中有两种是电解质 B、图中五个转化关系,有三个是化合反应
C、上述所涉及的化合物的晶体均是分子晶体 D、图中五个转化关系均为氧化还原反应
(4)用甲、丙、乙、硫酸溶液可以构成一原电池,则电极材料可以为______,正极的电极反应式为______.
Ⅱ.向某密闭容器中加入 0.4mol B、0.3mol D和一定量的A三种气体.一定条件下发生反应,各物质浓度随时间的变化如下图中甲图所示.乙图为 t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同条件,所用条件均不同.已知t3~t4阶段为使用催化剂[已知 t~t1阶段 c ( A)未画出].
(1)A的起始物质的量为______;
(2)此条件下的化学平衡常数为______;
(3)t4~t5阶段改变的条件为______.
 查看习题详情和答案>>
查看习题详情和答案>>

