网址:http://m.1010jiajiao.com/timu_id_406051[举报]
一、1.解析:设原溶液中水的质量为w g,R的质量为 m g,R的溶解度为S g,则有:

根据比例性质,可设:?

S= ×100=
×100=
答案:B?
2.解析:注意体积效应。?
答案:B?
3.解析:因H2SO4溶液的密度随浓度增大而增大,是一个变值而不是一个定值。设稀释后溶液密度为ρ′,则有:18× ×10-3=9×
×10-3=9× ×10-3,2
×10-3,2 =
= ,因为
,因为
ρ′<ρ,故V<100(mL)。
答案:A?
4.解析:NH3+2O2===HNO3+H2O?
HNO3%= ×100%=78%
×100%=78%
答案:A
5.AB 6.B 7.B 8.D 9.C?
二、10.
11.
 g
g
12.(1)G、E、C、H、F(或E、G、C、H、F)?
(2)BCD
14.(1)0.0813 mol?L-1 (2)32 mL?
15.(1)四种?
①KOH,K2CO3 ②K2CO3 ③K2CO3,KHCO3?④KHCO3?
(2)解:2KOH+CO2 === K2CO3+H2O?
22.4 138?
2.24 x=13.8?
KOH+CO2===KHCO3?
22.4 100?
2.24 x=10.0?
从上面两方程知:生成的固体全部是K2CO3时应该是 =0.100 mol
=0.100 mol
若K2CO3为a mol,则KHCO3为(0.100-a)mol?
则得方程
即K2CO3和KHCO3各为0.050 mol?
K2CO3为:
KHCO3为:
依K+守恒的要求,设KOH溶液浓度为c则:?
0.300 Lc=0.050 mol×2+0.050 mol c=0.50 mol?L-1
(1)该气体的物质的量=
(2)若取上述氨水30.0mL与70.0mL2.00mol?L-1的AlCl3溶液相混合,产生白色沉淀的质量是
(3)若取某浓度的NaOH溶液50.0mL与50.0mL2.00mol?L-1的AlCl3溶液相混合,有白色沉淀产生,测得溶液中铝元素与沉淀中铝元素质量相等,则NaOH溶液的物质的量浓度为

(一)该硫酸的物质的量浓度为
(二)实验室用该硫酸配制240mL0.46mol/L的稀硫酸,则
(1)需要该硫酸的体积为
(2)有以下仪器:①烧杯②100mL量筒③250mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)⑦10mL量筒⑧胶头滴管,配制时,必须使用的仪器有
(3)配制过程中有几个关键的步骤和操作如下图所示:将上述实验步骤A-F按实验过程先后次序排列

(4)该同学实际配制得到的浓度为0.45mol/L,可能的原因是
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度.
 用氯化铁浸出重铬酸钾(K2Cr2O7)滴定法测定钛精粉试样中单质铁的质量分数[ω(Fe)%],实验步骤如下:
用氯化铁浸出重铬酸钾(K2Cr2O7)滴定法测定钛精粉试样中单质铁的质量分数[ω(Fe)%],实验步骤如下:步骤1:称取试样0.100g于250mL洗净的锥形瓶中.
步骤2:加入FeCl3溶液100mL,迅速塞上胶塞,用电磁搅拌器30min.
步骤3:过滤,用水洗涤锥形瓶和滤渣各3~4次,洗液全部并入滤液中.
步骤4:将滤液稀释至500mL,再移去100mL稀释液于锥形瓶中,加入20mL硫酸和磷酸的混合酸,加0.5%二苯胺磺酸钠指示剂4滴.
步骤5:以K2Cr2O7标准溶液滴定至出现明显紫色为终点.发生的反应为:Cr2O72-+6Fe2++14H+=2Cr3++Fe3++7H2O.
步骤6:重复测定两次.
步骤7:数据处理.
(1)步骤2中加入FeCl3溶液后锥形瓶中发生反应的离子方程式为
(2)步骤3中判断滤纸上残渣已洗净的方法是
(3)实验中需用到100mL浓度为0.01mol?L-1K2Cr2O7标准溶液,配置时用到的玻璃仪器有
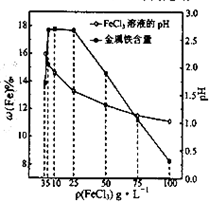
(4)科研人员确定FeCl3溶液的最佳浓度,选用100mL不同浓度的FeCl3溶液(FeCl3溶液均过量)溶解同一钛精粉试样,其余条件控制相同,得到测定结果如图所示.则FeCl3溶液的浓度[用ρ(FeCl3)表示]范围应为