摘要:关于m g H2和n g He的下列说法中.正确的是A.同温同压下.H2与He的体积比为m∶2n?B.同温同压下.若m=n.则H2与He的分子数之比为2∶1
网址:http://m.1010jiajiao.com/timu_id_406016[举报]
一、1.BD 2.AD 3.A?
4.解析:2CO+O2 2CO2 ΔV
2CO2 ΔV
2 1 2 1
50 mL
若O2过量:V(CO)=100 mL;若CO过量:V(O2)=50 mL则V(CO)=150 mL。
答案:AB?

则CO%=50%。
答案:A
6.D 7.B 8.D 9.A?
二、10.(1)V(CO)=2(m-n)L V(O2)=(2n-m)L V(CO)=n L
V(O2)=(m-n)L?
(2)CO2、CO
11.BD
12.(1)672 mL (2)76 g?mol-1?
13.N2O NO 1∶4?
14.(1)t℃、p Pa时D的密度a g?L-1?
m(C)=30.5 g-a g?L-1×3 L=(30.5-3 a)g?
(2)盐酸的浓度b mol?L-1?
若Mg过量,V(H2)= ×22.4 L?mol-1
×22.4 L?mol-1
若HCl过量:
V(H2)= ×22.4 L?mol-1?
×22.4 L?mol-1?
若正好完全反应,V(H2)上述两值等效,均可。?
15.(1)4∶3 (2)0.91 g/L?
16.(1)1 固体的量增加,产生气体的量增加,说明在1中有酸剩余。?
(2)固体为Na2CO3和NaHCO3的混合物:
Na2CO3%=55.79% NaHCO3%=44.21%?
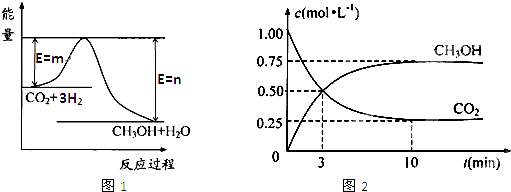
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ?mol-1)的变化.
(1)写出该反应的热化学方程式
(2)关于该反应的下列说法中,正确的是
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(3)该反应的平衡常数K的表达式为:
.
(4)温度降低,平衡常数K
(5)为探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=
(6)下列措施中能使n(CH3OH)/n(CO2)增大的有
A.升高温度 B.加入催化剂
C.将H2O(g)从体系中分离 D.充入He(g),使体系总压强增大.
查看习题详情和答案>>

(1)写出该反应的热化学方程式
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-(n-m)kJ?mol?1
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-(n-m)kJ?mol?1
.(2)关于该反应的下列说法中,正确的是
C
C
.A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(3)该反应的平衡常数K的表达式为:
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
(4)温度降低,平衡常数K
增大
增大
(填“增大”、“不变”或“减小”).(5)为探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=
0.225mol/(L.min)
0.225mol/(L.min)
.(6)下列措施中能使n(CH3OH)/n(CO2)增大的有
C
C
.A.升高温度 B.加入催化剂
C.将H2O(g)从体系中分离 D.充入He(g),使体系总压强增大.