摘要:3,(6)W1:(W-W1)或W1:133.5W2/78
网址:http://m.1010jiajiao.com/timu_id_405897[举报]
(2012?大兴区一模)下表为元素周期表的一部分,请参照①-⑨相关元素在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)由②④⑤三种元素组成的物质的水溶液显碱性,用离子方程式表示溶液显碱性的原因:
(4)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,则该化合物的电子式为:
 ,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:
,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:
(5)以⑥的单质材料为阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成有吸附性的难溶物R,写出阳极生成R的电极反应式:
(6)化学方程式:A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应类型,A、B、X、Y是中学常见的物质,下列反应中A都为单质,请回答:
(ⅰ)若A为红色固体,在加热条件下反应产生有刺激性气味、有漂白作用的气体,写出检验该气体的方法
(ⅱ)若A为黑色粉末,少量A和B常温下反应生成的Y是无色气体,且Y无色,该气体在空气中易变成红棕色,写出常温下少量A和B反应的化学方程式:
(iii)若B为白色乳状物,且溶解度随温度的升高而降低,Y可做固体干燥剂,则该反应在工业上可用于制备
查看习题详情和答案>>
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | |||||
Na>Al>O
Na>Al>O
.(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
HNO3>H2CO3>H2SiO3
HNO3>H2CO3>H2SiO3
.(3)由②④⑤三种元素组成的物质的水溶液显碱性,用离子方程式表示溶液显碱性的原因:
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
(4)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,则该化合物的电子式为:


3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
| ||
(5)以⑥的单质材料为阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成有吸附性的难溶物R,写出阳极生成R的电极反应式:
Al-3e-=Al3+,Al3++3HCO3-═Al(OH)3↓+3CO2↑或Al-3e-+3HCO3-═Al(OH)3↓+3CO2↑
Al-3e-=Al3+,Al3++3HCO3-═Al(OH)3↓+3CO2↑或Al-3e-+3HCO3-═Al(OH)3↓+3CO2↑
(6)化学方程式:A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应类型,A、B、X、Y是中学常见的物质,下列反应中A都为单质,请回答:
(ⅰ)若A为红色固体,在加热条件下反应产生有刺激性气味、有漂白作用的气体,写出检验该气体的方法
将气体X通入品红溶液中,若品红溶液褪色,加热恢复红色,证明气体X是SO2
将气体X通入品红溶液中,若品红溶液褪色,加热恢复红色,证明气体X是SO2
(ⅱ)若A为黑色粉末,少量A和B常温下反应生成的Y是无色气体,且Y无色,该气体在空气中易变成红棕色,写出常温下少量A和B反应的化学方程式:
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
(iii)若B为白色乳状物,且溶解度随温度的升高而降低,Y可做固体干燥剂,则该反应在工业上可用于制备
漂白粉
漂白粉
.某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4?7H2O)和胆矾晶体(CuSO4?5H2O),其实验方案如图:
方案一:
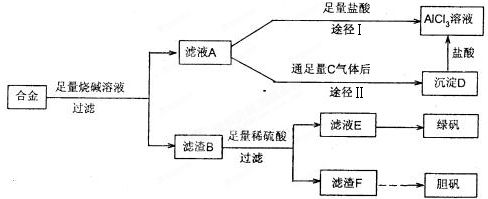
试回答下列问题:
(1)过滤用的器材已有:滤纸、铁架台、铁圈、烧杯和漏斗,还要补充的玻璃仪器是
(2)由滤液A制得AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是
(3)从滤液E中得到绿矾晶体的实验操作是
(4)写出用滤渣F制备胆矾晶体的化学方程式
方案二:
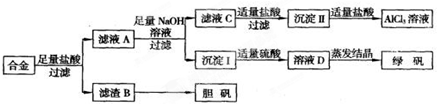
请回答下列问题:
(5)写出由滤液C到沉淀Ⅱ的离子方程式
(6)小组成员经过检测,发现制得的绿矾不纯,试分析原因
(7)方案一和方案二,你认为哪种方案相对
查看习题详情和答案>>
方案一:

试回答下列问题:
(1)过滤用的器材已有:滤纸、铁架台、铁圈、烧杯和漏斗,还要补充的玻璃仪器是
玻璃棒
玻璃棒
.(2)由滤液A制得AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是
Ⅱ
Ⅱ
,理由是按途径I直接向A加入盐酸得到的AlCl3溶液中含有大量的NaCl杂质
按途径I直接向A加入盐酸得到的AlCl3溶液中含有大量的NaCl杂质
.(3)从滤液E中得到绿矾晶体的实验操作是
蒸发浓缩、冷却结晶、洗涤、干燥
蒸发浓缩、冷却结晶、洗涤、干燥
.(4)写出用滤渣F制备胆矾晶体的化学方程式
2Cu+O2+2H2SO4=2CuSO4+2H2O
2Cu+O2+2H2SO4=2CuSO4+2H2O
,CuSO4+5H2O=CuSO4?5H2O
CuSO4+5H2O=CuSO4?5H2O
.方案二:

请回答下列问题:
(5)写出由滤液C到沉淀Ⅱ的离子方程式
H2O+AlO2-+H+=Al(OH)3↓
H2O+AlO2-+H+=Al(OH)3↓
.(6)小组成员经过检测,发现制得的绿矾不纯,试分析原因
亚铁离子易被氧化为三价铁离子
亚铁离子易被氧化为三价铁离子
,小组成员检测制得的绿矾不纯所用试剂为KSCN溶液
KSCN溶液
.(7)方案一和方案二,你认为哪种方案相对
方案一
方案一
更合理,理由是酸的量的控制上没有过高的要求,只需过量即可,但是方案二中,适量的酸没法控制
酸的量的控制上没有过高的要求,只需过量即可,但是方案二中,适量的酸没法控制
.