网址:http://m.1010jiajiao.com/timu_id_405554[举报]
(一)选择题
1.D 2.C 3.C 4.D 5.C 6.D 7.B、C 8.B 9.C 10.A 11.B 12.C、D 13.C、D 14 .B、C 15.B 16.D 17.D 18.D 19.B 20.C 21.A 22.A、B 23.B 24.D 25.D
(二)非选择题
1.答案为有机物的推断.files/image260.jpg)
2.(1)(A)4 (B)7 (C)5 (2)(D)4 (E)4 (F)2
3.(1)N2H4, 有机物的推断.files/image261.gif)
(2)H2N-NH2+H2O有机物的推断.files/image262.gif) H2N-NH2?H2O
H2N-NH2?H2O
H2N-NH2?H2O+H2O有机物的推断.files/image262.gif) H2O?H2N-NH2?H2O
H2O?H2N-NH2?H2O
4.(1)NxHy+有机物的推断.files/image121.gif) O2
O2有机物的推断.files/image123.gif)
有机物的推断.files/image264.gif) N2+
N2+有机物的推断.files/image125.gif) H2O (2)N2H4
H2O (2)N2H4
5.(1)略 (2)14.7 (3)NOx(或NO、NO2)、CO.
6.(1)23.3% (2)1.26×1018kJ (3)A=[有机物的推断.files/image267.gif) ×6×
×6×有机物的推断.files/image269.gif) Q为每生成1 mol葡萄糖所需要吸收的能量(或:每消耗6 mol CO2所需吸收的能量)
Q为每生成1 mol葡萄糖所需要吸收的能量(或:每消耗6 mol CO2所需吸收的能量)
7.(1)b、c、b、c、b (2)NaOH―CH3CH2OH溶液、加热
(3)有机物的推断.files/image270.gif)
8.(1)甲酸甲酯,HCHO,有机物的推断.files/image272.gif)
(2)CH3COONa+NaOH有机物的推断.files/image190.gif) Na2CO3+CH3↑
Na2CO3+CH3↑
(3)有机物的推断.files/image274.gif) (或
(或 有机物的推断.files/image276.gif) ,
,
有机物的推断.files/image278.gif)
有机物的推断.files/image280.gif)
9.(1)3∶2∶3 (2)有机物的推断.files/image282.jpg)
10.(1)CH2O (2)30,60;CH2O,C2H4O2
有机物的推断.files/image284.jpg)
有机物的推断.files/image286.jpg)
14.(1)乙二醇,乙二酸
(2)①,②,④ (3)②,④
(4)有机物的推断.files/image288.gif)
有机物的推断.files/image290.jpg)
17.(1)有机物的推断.files/image292.gif) 40%
40%
(2)CH3CH2CH2CHO,(CH3)2CHCHO,有机物的推断.files/image294.gif)
(3)CH2=CHCH(CH3)2
18.(1)2ClCH2COO?-2e有机物的推断.files/image123.gif) ClCH2CH2Cl+2CO2
ClCH2CH2Cl+2CO2
2H2O+2e有机物的推断.files/image123.gif) H2+2OH-
H2+2OH-
(2) 有机物的推断.files/image296.gif)
(3) 有机物的推断.files/image298.gif)
有机物的推断.files/image300.gif)
? 有机物的推断.files/image302.gif) ?n
?n
19.(1)CaC2+2H2O有机物的推断.files/image123.gif) Ca(OH)2+C2H2↑
Ca(OH)2+C2H2↑
(2)CH≡CH+H2有机物的推断.files/image123.gif) CH2=CH2
CH2=CH2
(3)CH2=CH2+HCl有机物的推断.files/image123.gif) CH3CH2Cl
CH3CH2Cl
有机物的推断.files/image303.gif)
20.(1)n(C)=0.160(mol) n(H)=0.120(mol) n(O)=0.08(mol)
(2)最简式为C4H3O2.
(3)有机物的推断.files/image304.gif)
21.(1)4
(2)C4H6O4 (3)5, 有机物的推断.files/image306.gif)
(4)CH3OH, C2H5OH,H2O
22.A:CH―CH3―CH3,B:CH2―CH3―CH2OH,C:CH3CH2―O―CH3;A∶B∶C=1∶3∶6
|
OH
O
‖
23.(1)CH4,CH3―C―CH3
(2)CH2=C―COOH+CH3OH有机物的推断.files/image308.gif) CH2=C―COOCH3+2H2O
CH2=C―COOCH3+2H2O
| |
CH3 CH3
(3)加成,取代
COOCH3
|
(4)nCH2=C-COOCH3有机物的推断.files/image123.gif) ?CH2―C?n
?CH2―C?n
| |
CH3 CH3
24.(1)CxHy+(有机物的推断.files/image310.gif) )O2
)O2有机物的推断.files/image123.gif) mCO2+
mCO2+有机物的推断.files/image125.gif) H2O+(x-m)CO (2)C4H8
H2O+(x-m)CO (2)C4H8
(3)
分子式
n(CO)∶n(CO2)
C3H8
1∶2
C4H6
1∶3
O
‖
25.(1)(略) (2)缩聚nCH3 ―CH―COOH有机物的推断.files/image313.gif) H?O―CH―C?n―OH+(n-1)H2O
H?O―CH―C?n―OH+(n-1)H2O
| |
OH OH
O
‖
(3)H?O―CH―C?nOH+(n-1)H2O有机物的推断.files/image308.gif) nCH3―CH―COOH
nCH3―CH―COOH
| |
OH OH
有机物的推断.files/image315.gif)
26.(1)6CO2+12H2O有机物的推断.files/image317.gif) C6H12O6+6H2O+6O2
C6H12O6+6H2O+6O2
(2)C+O2=CO2
CnH2n+2+有机物的推断.files/image319.gif) O2
O2有机物的推断.files/image123.gif) nCO2+(n+1)H2O
nCO2+(n+1)H2O
CH4+2O2=CO2+2H2O
CH4产生的CO2最小,对环境负面影响最小
27.(1)C9H10O2 (2)4
有机物的推断.files/image320.gif)
28.(1)O=C=C=C=O
O O
‖ ‖
(2)C3O2+2HCl有机物的推断.files/image123.gif) Cl―C―CH2―C―Cl]
Cl―C―CH2―C―Cl]
O O
‖ ‖
C3O2+有机物的推断.files/image123.gif) C2H5―C―CH2―C―OCH2
C2H5―C―CH2―C―OCH2
29.(1)C15H13O
有机物的推断.files/image322.jpg)
30.(1)A,B;C,F;D,E (2)都有18O标记。因为反应中间体在消去一分子H2O 时,有两种可能,而乙氧基(OC2H5)是保留的。
有机物的推断.files/image324.jpg)
(3)有机物的推断.files/image326.gif) (或答中间体) ,因为这个碳原子连有4个原子团。
(或答中间体) ,因为这个碳原子连有4个原子团。
31.(1)C6H5―CH―NH―CO―C6H5+H2O有机物的推断.files/image308.gif) C6H5―CH―NH2+C6H5COOH
C6H5―CH―NH2+C6H5COOH
| |
HO―CH―COOH HO―CH―COOH
(2)α (3)C31H38O11
32.(1)0.125;0.30;0.100;5:12:4
(2)可以;因为该最简式中H原子个数已经饱和,所以最简式即分子式C5H12O4
(3)C(CH2OH)4
33.(1)十肽 (2)4个谷氨酸 (3)3个苯丙氨酸

现准确称取0.44g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重0.88g,B管增重0.36g.请回答:
(1)按上述所给的测量信息,装置的连接顺序应是:D
(2)A、B管内均盛有有固态试剂,A管的作用是
(3)E中应盛装什么试剂:
(4)如果把CuO网去掉,A管重量将
(5)请改进这套装置的一个不足之处
(6)该有机物的实验式为
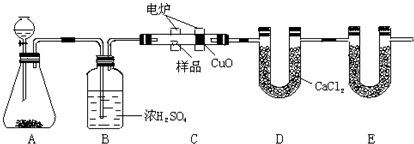
回答下列问题:
(1)A装置中分液漏斗盛放的物质是
| MnO2 |
| MnO2 |
(2)C装置(燃烧管)中CuO的作用是
(3)写出E装置中所盛放物质的名称
(4)若准确称取1.20g样品(只含C、H、O三种元素中的两种或三种).经充分燃烧后,E管质量增加1.76g,D管质量增加0.72g,则该有机物的最简式为
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+
| 1 |
| 2 |
试判断常温下,上述反应能否自发进行
②CH4(g)+2O2(g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?mol-1
③CH4(g)+CO2(g)=2CO(g)+2H2(g)△H3=247.3kJ?mol-1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=
(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/(mol?L-1) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
 此条件下,该反应达到化学平衡时,氮气的浓度为
此条件下,该反应达到化学平衡时,氮气的浓度为(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式
(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好
A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol?L-1,则pC=-lg(1×10-3)=3.某温度下,H2CO3溶液的pC-pH关系如图.

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为
(2)求此温度下H2CO3?H++HCO3-的电离平衡常数
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?L-1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3-?H++CO32-移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液

(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是
(2)C装置中浓硫酸的作用是
(3)D装置中MnO2的作用是
(4)燃烧管中CuO的作用是
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为
(6)用质谱仪测定其相对分子质量,得如图一所示的质谱图,则该有机物的相对分子质量为
(7)能否根据A的实验式确定A的分子式
(8)该物质的核磁共振氢谱如图二所示,则其结构简式为
①用PH试纸检验,表明溶液呈强酸性
②取部分溶液,加入少量的CCl4及数滴新制的氯水,振荡后CCl4层显紫红色
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成
④将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
根据上述实验事实确定并回答:
(1)在溶液中,肯定存在的有
(2)写出实验④中的离子反应方程式
| ||
| ||
(3)不能确定是否存在的离子有