摘要:正.负极判断(以Zn│H2SO4│Cu)原电池为例 负极: 正极: 总反应: . [实验装置]书选修4:P12 [思考]:观察导线中电子流向和溶液中离子迁移.盐桥中有哪些物质?盐桥起什么作用?
网址:http://m.1010jiajiao.com/timu_id_4054579[举报]
(1)1780年,意大利解剖学家伽伐尼在用银质手术刀触碰放在铁盘上的青蛙的时候,无意间发现青蛙腿部肌肉抽搐了一下,仿佛受到电流的刺激.如果只用一种金属器械去触动青蛙,就无此种反应.伽伐尼认为出现这种现象的原因是动物体内存在“生物电”.结合你所学的知识模拟该过程,下列哪种材质的手术刀触碰铁盘上的青蛙腿不会产生触动?
a 铝 b 陶瓷 c 塑料 d 铁
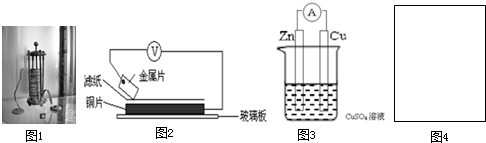
(2)1799年,伏打仔细研究了伽伐尼的发现,以含食盐水的湿抹布,夹在银和锌的圆形版中间,堆积成圆柱状,制造出世界上最早的电池-伏打电池(图1). 将洁净的金属片A、B、D、E分别放置在浸有盐溶液的滤纸上面并压紧(如图2所示).在每次实验时,记录电压表指针的移动方向和电压表的读数如下:
已知:构成两电极的金属其金属活泼性相差越大,电压表的读数越大.请依据表中数据判断:
(3)1836年,英国科学家丹尼尔对伏打电池进行改进,获得了世界上第一个能够获得稳定电流的电池,图3是丹尼尔电池的简易装置:
该电池的正极是
(4)随着社会的发展和科技的进步,越来越多的电池被制造出来.请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+以“ ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
查看习题详情和答案>>
bcd
bcd
(填字母)a 铝 b 陶瓷 c 塑料 d 铁

(2)1799年,伏打仔细研究了伽伐尼的发现,以含食盐水的湿抹布,夹在银和锌的圆形版中间,堆积成圆柱状,制造出世界上最早的电池-伏打电池(图1). 将洁净的金属片A、B、D、E分别放置在浸有盐溶液的滤纸上面并压紧(如图2所示).在每次实验时,记录电压表指针的移动方向和电压表的读数如下:
| 金属 | 电子流动方向 | 电压(V) |
| A | A→Cu | +0.78 |
| B | Cu→B | -0.15 |
| D | D→Cu | +1.35 |
| E | E→Cu | +0.30 |
D
D
金属可能是最强的还原剂;B
B
金属一定不能从硫酸铜溶液中置换出铜.(3)1836年,英国科学家丹尼尔对伏打电池进行改进,获得了世界上第一个能够获得稳定电流的电池,图3是丹尼尔电池的简易装置:
该电池的正极是
铜
铜
,负极是锌
锌
,正极反应是Cu2++2e-=Cu
Cu2++2e-=Cu
,负极反应是Zn-2e-=Fe2+
Zn-2e-=Fe2+
.(4)随着社会的发展和科技的进步,越来越多的电池被制造出来.请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+以“
 ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.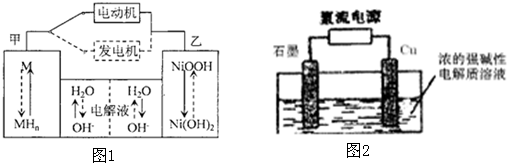
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH
(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
Cu2O+H2阴极的电极反应式是
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
查看习题详情和答案>>

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g),△H=-5121.9KJ/mol
| 25 |
| 2 |
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g),△H=-5121.9KJ/mol
.| 25 |
| 2 |
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
| 放电 |
| 充电 |
增大
增大
(填“增大”、“减小”或“不变”),该电极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-
NiOOH+H2O+e-=Ni(OH)2+OH-
.(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
| ||
2H++2e-=H2↑
2H++2e-=H2↑
.用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为144
144
g.(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
吸氧
吸氧
腐蚀.为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的负
负
极(填“正”或“负”)相连.第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为 .
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH (填“增大”、“减小”或“不变”),该电极的电极反应式为 .
(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
Cu2O+H2阴极的电极反应式是 .用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为 g.
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的 腐蚀.为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的 极(填“正”或“负”)相连.
查看习题详情和答案>>

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为 .
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
| 放电 |
| 充电 |
(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
| ||
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的 腐蚀.为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的 极(填“正”或“负”)相连.
第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为______.
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH 2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH______(填“增大”、“减小”或“不变”),该电极的电极反应式为______.
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH______(填“增大”、“减小”或“不变”),该电极的电极反应式为______.
(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O Cu2O+H2阴极的电极反应式是______.用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为______g.
Cu2O+H2阴极的电极反应式是______.用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为______g.
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的______腐蚀.为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的______极(填“正”或“负”)相连.
查看习题详情和答案>>

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为______.
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
 2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH______(填“增大”、“减小”或“不变”),该电极的电极反应式为______.
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH______(填“增大”、“减小”或“不变”),该电极的电极反应式为______.(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
 Cu2O+H2阴极的电极反应式是______.用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为______g.
Cu2O+H2阴极的电极反应式是______.用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为______g.(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的______腐蚀.为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的______极(填“正”或“负”)相连.
查看习题详情和答案>>