网址:http://m.1010jiajiao.com/timu_id_405014[举报]
一、1.B 2.D 3.D?
4.解析:FexOy+yCO xFe+yCO2?
xFe+yCO2?
(56x+16y) g y mol?
 mol
mol
得:x∶y=2∶3?
答案:B
5.AD 6.B 7.B 8.CD?
9.解析:A.如AlO B.如C+FeO
B.如C+FeO CO↑+Fe C.如Br-
CO↑+Fe C.如Br- Br2 D.如Fe3+
Br2 D.如Fe3+ Fe2+
Fe2+
答案:AD?
10.C?
二、11.FeCO3在空气中加热,因+2价铁被空气氧化而得不到FeO;而FeC2O4分解,产生的CO可作保护气,防止FeO氧化。?
12.(1)普通铁粉(或铁粉) 作为水蒸气发生器(或用来产生水蒸气) 防止水倒吸(或用作安全瓶) 氢气?
(2)固体NaOH(或碱石灰、CaO等碱性固体干燥剂) 6摩/升HCl?
注:G中如填写酸性干燥剂或液体干燥剂,则此空不给分。?
(3)ABE (必须全对给一分,错、漏一个即不给分)?
(4)加快氢气产生的速度?
(5)Fe3O4+4H2 3Fe+4H2O?
3Fe+4H2O?
(6)检验氢气的纯度 点燃氢气?
13.(1)A.浓NaOH溶液 B.NH4Cl固体 C.碱石灰 X:NH3?
(2)NaOH+NH4Cl NaCl+NH3↑+H2O?
NaCl+NH3↑+H2O?
2NH3+3CuO 3Cu+N2↑+3H2O?
3Cu+N2↑+3H2O?
14.(1)20.4% (2)BaO?Fe2O3?
15.Cu2O和Cu w(Cu2O)=42.9% w(Cu)=57.1%
 (2012?西安一模)已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期.A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体.
(2012?西安一模)已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期.A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体.(1)写出A元素的基态原子价电子排布式
(2)写出X的化学式
(3)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:
(4)CE、FA的晶格能分别为786KJ/mol l、3401KJ/mo,试分析导致两者晶格能差异的主要原因是:
(5)F与B可形成离子化合物,其晶胞结构如图所示:F与B形成离子化合物的化学式为
| 4×78g/mol |
| ag/cm3.6.02×1023/mol |
| 4×78g/mol |
| ag/cm3.6.02×1023/mol |
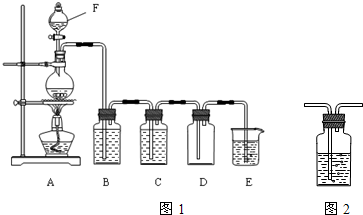
(1)装置F的名称是
(2)装置B中盛放的试剂是
(3)写出E中发生反应的化学方程式:
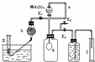
(4)图2装置是洗气瓶,该装置在化学实验中除洗气外,还有多种用途,试再写出其一种用途:
(5)实验室有时用高锰酸钾代替二氧化锰,与浓盐酸反应制取氯气,反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
若15.8g KMnO4与足量的浓盐酸充分反应,则有
 过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用.
过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用.已知:过碳酸钠与硫酸溶液反应的化学方程式如下:
Na2CO4+H2SO4→Na2SO4+H2O2+CO2↑ 2H2O2→2H2O+O2↑
为测定已变质的过碳酸钠(含碳酸钠)的纯度,设计如图所示的实验:Q为-具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中.
(1)Q内发生反应生成的气体为
(2)为测出反应时生成气体的总体积,滴稀H2SO4前必须关闭
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是
(4)实验结束时,量筒I中有xmL水,量筒Ⅱ中收集到ymL气体(上述体积均已折算到标准状况),则过碳酸钠的纯度是
(5)某同学实验测得的过碳酸钠的纯度超过100%,你认为可能的原因是
A.气体滞留在Q和导气管中,未全部进入量筒Ⅱ
B.量筒Ⅱ读数时,量筒液面高于水槽液面
C.右侧量筒Ⅰ和储液集气瓶连接导管内的液体没有计入读数x
D.气体体积数值x、y没有扣除滴加的硫酸的体积.
为了验证该同学的推断是否正确,甲、乙、丙三位同学各设计了一个实验方案.
甲同学的方案:将盛绿色溶液的试管加热,看是否有红棕色的气体产生.
(1)你认为甲同学的方案的不妥之处是什么?
乙同学的方案:用双氧水和二氧化锰制得氧气,并把氧气通入绿色溶液中,观察其溶液是否变蓝色.
(2)请用化学方程式表示其中的化学反应原理
丙同学的方案:在通风橱内,将一根下端弯成螺旋状且可抽动的铜丝插入盛有足量浓硝酸的试管A中,立即可观察到试管中充满红棕色的NO2气体.将NO2气体经导管通入到倾斜的另一支装有淡蓝色Cu(NO3)2溶液的试管B中,随着实验进行,试管B中的溶液蓝色加深,很快又转变为绿色,继续通入NO2,绿色保持不变,向上抽起铜丝,使反应停止.
(3)简述丙同学的方案中的溶液变色的原因.
(4)从环保的角度看,你认为三个方案中最好的是哪一个?说明理由.
(15分)
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果。某兴趣小组通过实验研究MnO2的性质
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是 。
| A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红 |
| B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红 |
| C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2观察是否有白色沉淀生成 |
| D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成 |
| 实验 | 酸或碱 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸溶液 | 迅速变棕褐色 |
写出在酸性条件下,MnO2氧化I-的离子方程式 。
(3)欲探究MnO2的催化效果,需要用30%的H2O2溶液(密度近似为1g/cm3)配制浓度3%的H2O2溶液(密度近似为1g/cm3)100mL。其配制方法是:用量筒量取 mL30%H2O2溶液放入 (填仪器名称)中,再加入一定量的水,搅拌均匀。
(4)在实验时,某同学把1滴KI溶液误滴入到过量的5mL3%的H2O2溶液中,发现产生了大量气泡。该小组查阅到KI与H2O2可发生如下反应:2KI+H2O2=KOH+I2,认为有可能是反应产物I2起了催化H2O2分解的作用。请设计一个简单实验证明该假设是否正确。
。
(5)实验室用二氧化锰和浓盐酸制取氯气,下列仪器可作为该反应的反应容器的是 (填序号)。




A B C D
(6)二氧化锰可用于制作干电池,电池总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,则其正极的电极反应式为 。 查看习题详情和答案>>