网址:http://m.1010jiajiao.com/timu_id_404954[举报]
一、1.解析:Fe Fe2+
Fe2+ Fe3+
Fe3+ Fe(OH)3
Fe(OH)3 Fe2O3。
Fe2O3。
答案:A?
2.B 3.C?
4.解析:根据2Fe3++Fe===3Fe2+知,消耗1 mol Fe生成3 mol Fe2+,还消耗2 mol Fe3+。
答案:C?
5.C 6.A 7.B 8.A 9.C 10.AD?
二、11.Fe2O3 CO和H2 Fe3O4、FeO?
12.(1)白色沉淀 灰绿色
灰绿色 红褐色沉淀?
红褐色沉淀?
(2)3Fe+2NO +8H+===3Fe2++2NO↑+4H2O?
+8H+===3Fe2++2NO↑+4H2O?
(3)由反应2HNO3+NO===3NO2+H2O知,在浓HNO3中不可能生成NO?
13.(1)Fe Cl2 H2?
(2)2Fe+3Cl2 2FeCl3
2FeCl3
(3)2HCl+Fe===FeCl2+H2↑?
(4)2FeCl2+Cl2===2FeCl3?
14.(1)Fe FeCl3 FeCl2 Fe(OH)3 Fe2O3 (2)略?
15.65 g 20.5%?
16.(1)ac?
(2)设Fe2O3原有n0 mol,还原百分率为A%,则有?


A%= ≈33.3%
≈33.3%
(3)3-
(4)Fe2O3、Fe3O4 8<a<9?
Fe3O4、FeO 6<a<8?
Fe2O3、Fe3O4、FeO 6<a<9
|
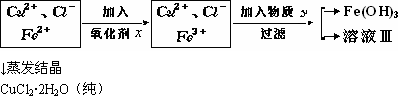
氯化铜(CuCl2·2H2O)中含FeCl2杂质.为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下面所示操作步骤进行提纯.
氧化剂x与物质Y的化学式分别是(已知完全成氢氧化物所需pH值:Fe3+为3.7,Cu2+为6.4,Fe2+为9.6.) | |
| [ ] | |
A. |
H2O2、CuO |
B. |
KMnO4、Na2O |
C. |
NaClO、Cu(OH)2 |
D. |
K2Cr2O7、NaOH |
(15分)工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
MnFe2O4的制备:
|
| 开始沉淀 | 完全沉淀 |
| Fe3+ | 2.7 | 3.7 |
| Mn2+ | 8.3 | 10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:
![]()
![]()
(3)由上可知,表示H2燃烧热的热化学方程式是__________________________。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
查看习题详情和答案>>
(15分)工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
MnFe2O4的制备:

|
|
开始沉淀 |
完全沉淀 |
|
Fe3+ |
2.7 |
3.7 |
|
Mn2+ |
8.3 |
10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:


(3)由上可知,表示H2燃烧热的热化学方程式是__________________________ 。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
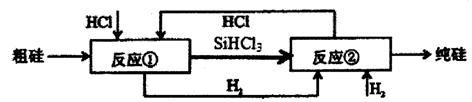
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
查看习题详情和答案>>
工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
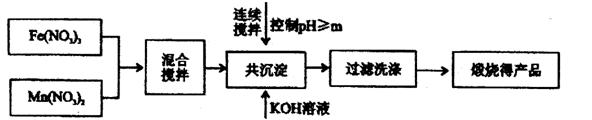
MnFe2O4的制备:
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 3.7 |
| Mn2+ | 8.3 | 10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:
![]()
![]()
(3)由上可知,表示H2燃烧热的热化学方程式是__________________________ 。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
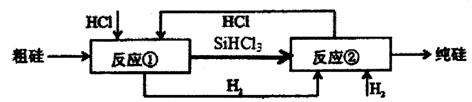
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
查看习题详情和答案>>