摘要:14.在2H2SO4(浓)+ Cu ====CuSO4+SO2↑ + 2H2O反应中.还原剂与氧化剂物质的量之比为 A.32∶49 B.1∶1 C.1∶2 D.2∶1
网址:http://m.1010jiajiao.com/timu_id_4039636[举报]
在Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O反应中
(1)
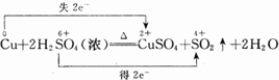
(2)用双线桥标出该反应电子转移的方向和数目.Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
(3)若有2.4mol的H2SO4参与反应,则被还原的H2SO4为
查看习题详情和答案>>
| ||
(1)
铜
铜
元素被氧化,硫酸
硫酸
是氧化剂.(2)用双线桥标出该反应电子转移的方向和数目.Cu+2H2SO4(浓)
| ||
(3)若有2.4mol的H2SO4参与反应,则被还原的H2SO4为
117.6
117.6
g.在Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O反应中
CuSO4+SO2↑+2H2O反应中
(1)______ 元素被氧化,______ 是氧化剂.
(2)用双线桥标出该反应电子转移的方向和数目.Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)若有2.4mol的H2SO4参与反应,则被还原的H2SO4为______ g.
查看习题详情和答案>>
(1)在Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O反应中,若有3.2 g的Cu参与反应,则被还原的H2SO4的物质的量是________mol.
CuSO4+SO2↑+2H2O反应中,若有3.2 g的Cu参与反应,则被还原的H2SO4的物质的量是________mol.
(2)下图是我校化学实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.计算:(要求写出简要计算过程)

①求该浓硫酸的物质的量浓度?
②用该浓硫酸配制200 mL 1 mol/L的稀硫酸,量筒所需量取该浓硫酸的体积是多少mL?