摘要:已知偶函数在区间单调递增.则满足<的x 取值范围是 (A).(.) (B). [.) (C). (.) (D). [.)
网址:http://m.1010jiajiao.com/timu_id_4037044[举报]
下表是某地市场销售的一种“加碘食盐”包装袋上的部分文字说明.
(1)已知碘在碘酸钾中的化合价为+5,碘酸钾的化学式为
(2)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是
(3)用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式为
该反应中氧化剂是:
查看习题详情和答案>>
| 配 料 | 氯化钠、碘酸钾 |
| 含碘量 | (20mg~40mg)/1kg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、防潮 |
KIO3
KIO3
.(2)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是
受热分解(热不稳定)
受热分解(热不稳定)
.(3)用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式为
I2+2KClO3═2KIO3+Cl2
I2+2KClO3═2KIO3+Cl2
.该反应中氧化剂是:
KClO3
KClO3
氧化产物是:KIO3
KIO3
,若有0.2molCl2产生,则转移电子的物质的量为2mol
2mol
.已知NaHSO4在水中的电离方程式为:NaHSO4═Na++H++SO42-.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2.下列对该溶液的叙述中,不正确的是( )
查看习题详情和答案>>
(2009?静安区二模)汽油中支链烃和环烃越多,汽油质量越高,通常用辛烷(2,2,3,3-四甲基丁烷)值来表示汽油质量.辛烷值越高,汽油的质量就越高.无铅汽油通常是加入甲基叔丁基醚作为高辛烷值组成.甲基叔丁基醚难溶于水.用以下两种方案制甲基叔丁基醚.
方案甲:
方案乙:
(1)叔丁醇的系统命名为
(2)已知醇在铜的催化下可发生氧化反应,如 试推测叔丁醇是否能发生类似反应
试推测叔丁醇是否能发生类似反应
(3)已知CH3CH2OH有3种不同化学环境的氢原子,则叔丁醇有
(4)方案乙不如方案甲,因为方案乙会发生两种类型的副反应,生成
 、
、
 (写结构简式)等副产品.
(写结构简式)等副产品.
(5)甲方案中,分离两种生成物以得到甲基叔丁基醚粗产品的方法是
a.水洗分液法 b.蒸馏法 c.过滤法.
查看习题详情和答案>>
方案甲:

方案乙:

(1)叔丁醇的系统命名为
2-甲基-2-丙醇
2-甲基-2-丙醇
;它有4种醇类同分异构体,写出其中一种的结构简式CH3CH2CH2CH2OH等
CH3CH2CH2CH2OH等
,它还有多种醚类同分异构体,其中一种可由乙醇在浓硫酸作用下分子间脱水生成,其结构简式为CH3CH2OCH2CH3
CH3CH2OCH2CH3
.(2)已知醇在铜的催化下可发生氧化反应,如
 试推测叔丁醇是否能发生类似反应
试推测叔丁醇是否能发生类似反应不能
不能
(填“能”、“不能”).(3)已知CH3CH2OH有3种不同化学环境的氢原子,则叔丁醇有
1
1
种不同化学环境的氢原子.(4)方案乙不如方案甲,因为方案乙会发生两种类型的副反应,生成
CH3OCH3
CH3OCH3
、



(5)甲方案中,分离两种生成物以得到甲基叔丁基醚粗产品的方法是
a
a
.a.水洗分液法 b.蒸馏法 c.过滤法.
随着化石能源的减少,新能源的开发利用日益迫切.
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
SO2(g)+I2(g)+2H2O(g)=2HI (g)+H2SO4(l)△H=a kJ?mol-1
2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g)△H=b kJ?mol-1
2HI(g)=H2(g)+I2(g)△H=c kJ?mol-1
则:2H2O(g)=2H2(g)+O2(g)△H= kJ?mol-1
(2)甲醇制氢有以下三个反应:
CH3OH(g)=CO(g)+2H2(g)△H=+90.8kJ?mol-1 Ⅰ
CO(g)+H2O(g)=CO2(g)+H2(g)△H=-43.5kJ?mol-1 Ⅱ
CH3OH(g)+
O2(g)=CO2(g)+2H2(g)△H=-192.0kJ?mol-1 Ⅲ
①当CH3OH(g)、O2(g)、H2O(g)总进料量为1mol时,且n(CH3OH):n(H2O):n(O2)=0.57:0.28:0.15,在0.1MPa、473~673K温度范围内,各组分的平衡组成随温度变化的关系曲线见图.(图中Yi表示各气体的体积分数,氧气的平衡浓度接近0,图中未标出).下列说法正确的是 .
A.在0.1MPa、473~673K温度范围内,甲醇有很高的转化率
B.温度升高有利于氢气的制备
C.寻找在较低温度下的催化剂在本制氢工艺中至关重要
②已知反应Ⅱ在T1℃时K=1,向恒容的密闭容器中同时充入1.0mol CO、3.0molH2O,达到平衡时CO的转化率为 .在反应达到平衡后再向其中加入1.0mol CO、1.0mol H2O、1.0mol CO2和1.0mol H2,此时该反应的v正 v逆(填“>”、“<”或“=”).
(3)一种以甲醇作燃料的电池示意图见图.写出该电池放电时负极的电极反应式: .
(4)LiBH4有很高的燃烧热,可做火箭的燃料,写出其燃烧反应的化学方程式: .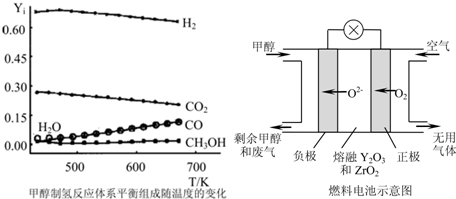
查看习题详情和答案>>
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
SO2(g)+I2(g)+2H2O(g)=2HI (g)+H2SO4(l)△H=a kJ?mol-1
2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g)△H=b kJ?mol-1
2HI(g)=H2(g)+I2(g)△H=c kJ?mol-1
则:2H2O(g)=2H2(g)+O2(g)△H=
(2)甲醇制氢有以下三个反应:
CH3OH(g)=CO(g)+2H2(g)△H=+90.8kJ?mol-1 Ⅰ
CO(g)+H2O(g)=CO2(g)+H2(g)△H=-43.5kJ?mol-1 Ⅱ
CH3OH(g)+
| 1 | 2 |
①当CH3OH(g)、O2(g)、H2O(g)总进料量为1mol时,且n(CH3OH):n(H2O):n(O2)=0.57:0.28:0.15,在0.1MPa、473~673K温度范围内,各组分的平衡组成随温度变化的关系曲线见图.(图中Yi表示各气体的体积分数,氧气的平衡浓度接近0,图中未标出).下列说法正确的是
A.在0.1MPa、473~673K温度范围内,甲醇有很高的转化率
B.温度升高有利于氢气的制备
C.寻找在较低温度下的催化剂在本制氢工艺中至关重要
②已知反应Ⅱ在T1℃时K=1,向恒容的密闭容器中同时充入1.0mol CO、3.0molH2O,达到平衡时CO的转化率为
(3)一种以甲醇作燃料的电池示意图见图.写出该电池放电时负极的电极反应式:
(4)LiBH4有很高的燃烧热,可做火箭的燃料,写出其燃烧反应的化学方程式:

 已知X、Y、Z、W四种短周期元素的原子半径依次减小.在周期表中X与Y、Y与Z均位同一周期的相邻位置;X的最外层电子数为次外层电子数的2倍;W分别能与X、Y、Z按一定原子数比形成电子总数为10的常见化合物.请判断X、Y、Z、W四种元素并回答下列问题:(要求用确定后的元素符号及有关化学用语表示)
已知X、Y、Z、W四种短周期元素的原子半径依次减小.在周期表中X与Y、Y与Z均位同一周期的相邻位置;X的最外层电子数为次外层电子数的2倍;W分别能与X、Y、Z按一定原子数比形成电子总数为10的常见化合物.请判断X、Y、Z、W四种元素并回答下列问题:(要求用确定后的元素符号及有关化学用语表示)(1)(XY)2分子中所有原子最外层都满足8电子,请写出其结构式:
(2)已知乙炔在一定条件下可以三聚生成苯:
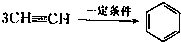 三聚氰胺也可以由氰胺(WXY分子中的W原子被氨基取代后可得氰胺)发生类似于乙炔的三聚反应而得到,三聚氰胺中无非极性键,含有量个氨基.请写出三聚氰胺结构简式:
三聚氰胺也可以由氰胺(WXY分子中的W原子被氨基取代后可得氰胺)发生类似于乙炔的三聚反应而得到,三聚氰胺中无非极性键,含有量个氨基.请写出三聚氰胺结构简式:(3)三聚氰胺遇强簸或强碱水溶液发生水解,氨基逐步被羟基取代生成三聚氰酸.三聚氰胺由于含氮量高而被一些奶粉厂家非法掺人奶粉中以提高其产品的含氮量(俗称蛋白精),经研究表明三聚氰胺和三聚氰酸在肾细胞中结合沉积从而形成肾结石,堵塞肾小管,最终造成肾衰竭,严重则危及生命.试写出三聚氰胺生成三聚氰酸的化学方程式:
(4)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将XZ2转化成有机物实现碳循环.如:2XZ2(g)+2W2Z(l)═X2W4(g)+3Z2(g)△H=+1411.0kJ/mol;2XZ2(g)+3W2Z(l)═X2W5ZW(l)+3Z2(g)△H=+1366.8kJ/mol则由X2W4水化制X2W5ZW反应的热化学方程式为
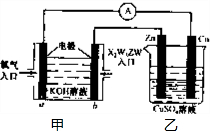
(5)利用X2W5ZW燃料电池设计如图所示的装置:
①则该装置中Cu极为
②写出b极的电极反应式为
③当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为