摘要:下列制取硫酸铜的实验设计中.能体现“经济.高效.环保 精神的最佳方案是( ) A.铜与浓硫酸供热 B.用铜片为阳极.石墨为阴极.电解稀硫酸 C.先灼烧废铜屑生成氧化铜.然后再用浓硫酸溶解 D. 适当温度下.使铜片在持续通入空气的稀硫酸中溶解 [解析]选D.本题考查实验设计.较易题.由反应原理可知.选项D符合条件.
网址:http://m.1010jiajiao.com/timu_id_4034795[举报]
(2010?惠州模拟)ClO2是一种常用的预防“禽流感”的消毒剂,可通过以下反应制得(未配平):KClO3+H2C2O4+H2SO4→ClO2↑+K2SO4+CO2↑+H2O
下列说法正确的是( )
下列说法正确的是( )
查看习题详情和答案>>
(2010?惠州模拟)除杂时加入的试剂须稍加过量,最后过量的物质可用物理或化学方法除去.现要除去NaCl溶液中少量的CaCl2,Na2SO4,下列选用试剂及加入的顺序正确的是( )
查看习题详情和答案>>
(2010?惠州模拟)某同学对Cu的常见化合物的性质进行实验探究,研究的问题和过程如下:
①在周期表中Cu和Al位置比较接近,Al(OH)3具有两性,Cu(OH)2是否也有两性?
②通常情况下,+2价Fe不如十3价Fe稳定,十l价Cu也一定不如+2价Cu稳定吗?
③CuO有氧化性,能被H2、CO还原,CuO也能被NH3还原吗?
(I)为探究问题①,除Cu(OH)2外必须选用的试剂为
a、稀H2SO4 b、浓的NaOH溶液 c、浓氨水 (NH3.H2O)
(II)为探究问题②,进行如下实验:
(1)将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末,该反应的化学方程式为
(2)向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,+1价Cu比+2价Cu更
(III)为解决问题③,他设计了如下实验(夹持装置未画):
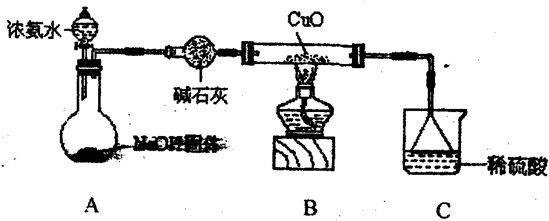
装置B中NH3和CuO反应生成铜,同时生成一种无污染的气体,反应的化学方程式为
查看习题详情和答案>>
①在周期表中Cu和Al位置比较接近,Al(OH)3具有两性,Cu(OH)2是否也有两性?
②通常情况下,+2价Fe不如十3价Fe稳定,十l价Cu也一定不如+2价Cu稳定吗?
③CuO有氧化性,能被H2、CO还原,CuO也能被NH3还原吗?
(I)为探究问题①,除Cu(OH)2外必须选用的试剂为
a、b
a、b
(填序号):a、稀H2SO4 b、浓的NaOH溶液 c、浓氨水 (NH3.H2O)
(II)为探究问题②,进行如下实验:
(1)将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末,该反应的化学方程式为
4CuO
2Cu2O+O2↑
| ||
4CuO
2Cu2O+O2↑
.该反应说明:在高温条件下,十l价的Cu比十2价Cu更
| ||
稳定
稳定
(填“稳定”或“不稳定”).(2)向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,+1价Cu比+2价Cu更
不稳定
不稳定
(填“稳定”或“不稳定”).(III)为解决问题③,他设计了如下实验(夹持装置未画):

装置B中NH3和CuO反应生成铜,同时生成一种无污染的气体,反应的化学方程式为
3CuO+2NH3
N2 ↑+3Cu+3H2O
| ||
3CuO+2NH3
N2 ↑+3Cu+3H2O
,说明CuO能够被NH3还原.装置C的作用:
| ||
充分吸收反应多余的NH3,并防止倒吸现象
充分吸收反应多余的NH3,并防止倒吸现象
. (2010?惠州模拟)如图A~D四种物质均含有同一种元素,A可以是单质也可以是气态氢化物,D是最高价氧化物对应的水化物,则A、B、C、D中共含有的元素是( )
(2010?惠州模拟)如图A~D四种物质均含有同一种元素,A可以是单质也可以是气态氢化物,D是最高价氧化物对应的水化物,则A、B、C、D中共含有的元素是( )