摘要:59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
网址:http://m.1010jiajiao.com/timu_id_4030831[举报]
为了测定大理石(假设大理石中的其它成分不参与反应,也不溶于水)样品中碳酸钙的质量分数,淘气同学取一定质量的大理石样品放入烧杯中,再取180g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
(1)淘气同学要用质量分数为36.5%浓盐酸配制所需的200克稀盐酸,则需浓盐酸的质量为
(2)上述反应的化学方程式为
(3)根据碳酸钙的质量列出求解第二次生成二氧化碳质量(x)的比例式
=
=
;
(4)向第四次反应后所得溶液中加8.8g水,则所得溶液中氯化钙的质量分数是
(5)用这样的大理石200t可以炼制含杂质20%的生石灰的质量是
查看习题详情和答案>>
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量(g) | 50 | 50 | 50 | 30 |
| 剩余固体的质量(g) | 17 | 9 | 5 | 5 |
64g
64g
(2)上述反应的化学方程式为
CaCO3+2HCl═CaCl2+CO2↑+H2O
CaCO3+2HCl═CaCl2+CO2↑+H2O
;(3)根据碳酸钙的质量列出求解第二次生成二氧化碳质量(x)的比例式
| 100 |
| 44 |
| 8g |
| x |
| 100 |
| 44 |
| 8g |
| x |
(4)向第四次反应后所得溶液中加8.8g水,则所得溶液中氯化钙的质量分数是
11.1%
11.1%
(5)用这样的大理石200t可以炼制含杂质20%的生石灰的质量是
112t
112t
. (2008?沐川县一模)如图是实验室用大理石与稀盐酸反应制取二氧化碳的实验装置图.请回答:
(2008?沐川县一模)如图是实验室用大理石与稀盐酸反应制取二氧化碳的实验装置图.请回答:(1)指出仪器名称:a
锥形瓶
锥形瓶
,b胶皮管
胶皮管
,c集气瓶
集气瓶
.(2)写出该反应的化学方程式:
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.(3)收集二氧化碳的方法是
向上排空气法
向上排空气法
,检验二氧化碳的方法是将燃着的木条放在集气瓶口,若木条熄灭则说明收集满了
将燃着的木条放在集气瓶口,若木条熄灭则说明收集满了
.(4)请列举出二氧化碳的用途(至少一种)
灭火
灭火
.某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取CO2.请你参与下列的探究并回答问题.
【提出问题】上述盐酸和碳酸盐的反应是否适合在实验室制取CO2?
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因
讨论后大家设计了如下三个实验进行对比分析.
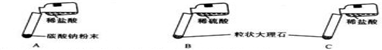
【实验与结论】(1)请你填写实验报告中①、②处的内容.
(2)根据探究结论,实验室制取二氧化碳的反应原理为
【拓展与迁移】(1)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:
查看习题详情和答案>>
【提出问题】上述盐酸和碳酸盐的反应是否适合在实验室制取CO2?
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因
浓盐酸易挥发,使制出的CO2不纯;
浓盐酸易挥发,使制出的CO2不纯;
.讨论后大家设计了如下三个实验进行对比分析.

【实验与结论】(1)请你填写实验报告中①、②处的内容.
| 实验 | 实验现象 | 实验内容 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止. | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ① 产生大量气泡 产生大量气泡 |
② 反应速率适中,气体便于收集 反应速率适中,气体便于收集 |
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
( 用化学方程式表示).【拓展与迁移】(1)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:
制出的气体要纯净
制出的气体要纯净
.31、实验室用大理石(杂质既不溶于水也不与稀盐酸反应)和稀盐酸反应制取二氧化碳.实验结束后,锥形瓶内已无气泡产生,但还有少量固体剩余.写出反应的化学方程式
小文和小明对锥形瓶内溶液中溶质的成分展开辩论:
小文说:因瓶内有固体剩余,所以溶液中只有氯化钙而无盐酸.小明不完全同意小文的说法,请你说出小明的理由

查看习题详情和答案>>
CaCO3+2HCl=CaCl2+H2O+CO2↑
,该反应的基本类型是
复分解反应
.小文和小明对锥形瓶内溶液中溶质的成分展开辩论:
小文说:因瓶内有固体剩余,所以溶液中只有氯化钙而无盐酸.小明不完全同意小文的说法,请你说出小明的理由
剩余的固体可能完全是杂质
.按小明的猜想,写出溶液中成分的几种可能
HCl和CaCl2或CaCl2
,请你选择其中-种情况,设计实验证明,完成下列探究报告:
14、实验室用大理石(杂质既不溶于水也不与稀盐酸反应)和稀盐酸反应制取二氧化碳.实验结束后,锥形瓶内已无气泡产生,但还有少量固体剩余.小文和小明对锥形瓶内溶液中溶质的成分展开辩论:
(1)小文说:因为瓶内有固体剩余,所以溶液中只有氯化钙而无盐酸.反应化学方程式为
(2)按小明的猜想,写出溶液中溶质成分的几种可能
(3)请你选择其中一种情况,设计实验证明,完成下列探究报告:
查看习题详情和答案>>
(1)小文说:因为瓶内有固体剩余,所以溶液中只有氯化钙而无盐酸.反应化学方程式为
CaCO3+2HCl═CaCl2+H2O+CO2↑
.小明不完全同意小文的说法,请你说出小明的理由盐酸过量,剩余固体可能完全是杂质
.(2)按小明的猜想,写出溶液中溶质成分的几种可能
CaCl2和HCl
;CaCl2
;(最少写两种)(3)请你选择其中一种情况,设计实验证明,完成下列探究报告:
| 猜想 | 实验步骤 | 实验现象及结论 |
氯化钙和盐酸 |
取少量,加石蕊试液 |
紫色石蕊试液变红,有盐酸和氯化钙 |