网址:http://m.1010jiajiao.com/timu_id_4029264[举报]
下面是某同学检验海水中溴离子的实验,请你参与他的探究:
(1)由于溴离子在海水中浓度很低(0.067g/L),要先取海水样品(设取50mL)进行浓缩,浓缩时下面的仪器______是不需要的(填编号):
A.玻璃棒 B.三脚架 C.酒精灯 D.蒸发皿 E.100mL烧杯
(2)取浓缩后的海水(假设剩余10mL左右)进行氧化和萃取.
①下列试剂都可以氧化浓缩后海水中的溴离子,实验中最好选______(填编号):
A.氯水 B.双氧水 C.酸性高锰酸钾溶液
②加入一定量氧化剂后,对氧化后的溶液进行假设和实验:
假设1:溶液中全部为Br-; 假设2:溶液全部为Br2
假设3:溶液中______.
③设计方案、进行实验,验证假设:请在表中写出实验步骤以及预期现象和结论(可以不填满).限选实验试剂和仪器:10mL量筒、小烧杯、试管、胶头滴管、分液漏斗;无水乙醇、裂化汽油、苯、0.10mol/LAgNO3、0.10mol/LHNO3
| 实验步骤 | 预期现象和结论 |
| 步骤1:用量筒取样品溶液6mL于分液漏斗中,再取______ | 若上层有机层出现橙色或橙红色,则假设2或假设3成立;______ |
| 步骤2:从分液漏斗放出______(上、下)层液于另一试管,______. | ______ |
(20分)草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:
称取Wg草酸晶体,配成100.00mL无色水溶液。量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定。试回答:
(1)滴定时所发生反应的化学方程式为
(2)草酸是二元弱酸,则草酸的电离方程式为 请从“电离平衡”的角度解释:为什么草酸的第二步电离比第一步难
(3)实验中不需要的仪器有(填序号)___________,还缺少的仪器有(填名称)______________________________。
a.托盘天平(带砝码,镊子) b.酸式滴定管 c.碱式滴定管 d.100mL容量瓶 e.烧杯
f.漏斗 g.锥形瓶 h.玻璃棒 i.药匙 j.烧瓶
图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是___________mL。图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_____________。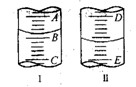
| A.是amL | B.是(25-a)mL | C.一定大于amL | D.一定大于(25-a)mL |
(5)在滴定过程中若用amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_____________mol·L-1;
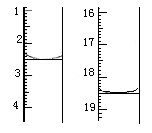
(6)若测得x=2,称取某二水合草酸晶体0.1200 g,加适量水完全溶解,然后用0.02000 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 。
 查看习题详情和答案>>
查看习题详情和答案>>
(1)由于溴离子在海水中浓度很低(0.067g/L),要先取海水样品(设取50mL)进行浓缩,浓缩时下面的仪器
A.玻璃棒 B.三脚架 C.酒精灯 D.蒸发皿 E.100mL烧杯
(2)取浓缩后的海水(假设剩余10mL左右)进行氧化和萃取.
①下列试剂都可以氧化浓缩后海水中的溴离子,实验中最好选
A.氯水 B.双氧水 C.酸性高锰酸钾溶液
②加入一定量氧化剂后,对氧化后的溶液进行假设和实验:
假设1:溶液中全部为Br-; 假设2:溶液全部为Br2
假设3:溶液中
③设计方案、进行实验,验证假设:请在表中写出实验步骤以及预期现象和结论(可以不填满).限选实验试剂和仪器:10mL量筒、小烧杯、试管、胶头滴管、分液漏斗;无水乙醇、裂化汽油、苯、0.10mol/LAgNO3、0.10mol/LHNO3
| 实验步骤 | 预期现象和结论 |
| 步骤1:用量筒取样品溶液6mL于分液漏斗中,再取 足量(过量)苯加入分液漏斗中,充分振荡,静置. 足量(过量)苯加入分液漏斗中,充分振荡,静置. |
若上层有机层出现橙色或橙红色,则假设2或假设3成立; 若上层有机层仍然为无色(或未出现橙红色),则假设1成立 若上层有机层仍然为无色(或未出现橙红色),则假设1成立 |
| 步骤2:从分液漏斗放出 2~3mL下 2~3mL下 (上、下)层液于另一试管,用胶头滴管滴加2~3滴0.10mol/LAgNO3 用胶头滴管滴加2~3滴0.10mol/LAgNO3 . |
若出现浅黄色沉淀,则假设3成立; 若没有浅黄色沉淀,则假设2成立. 若出现浅黄色沉淀,则假设3成立; 若没有浅黄色沉淀,则假设2成立. |
 铁及其化合物之间的相互转化可用下式表示:①②③④
铁及其化合物之间的相互转化可用下式表示:①②③④Fe2+
| ① |
| ④ |
| ② |
| ③ |
2- 4 |
(1)铁元素在周期表中的位置是
(2)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是
A.Cl2 B.Fe C.HNO3 D.H2O2
(3)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应CuFeS2+4Fe3+=Cu2++5Fe2++2S(CuFeS2中S为-2价),下列说法正确的是
A.从物质分类的角度看,黄铜矿属于合金
B.反应中,所有铁元素均被还原
C.反应中,CuFeS2 既作氧化剂又作还原剂
D.当转移1mol电子时,46g CuFeS2参加反应
(4)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:
FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(5)向某稀HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体,该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如图所示.则混合溶液中HNO3和Fe(NO3)3的物质的量浓度之比为
(6)某同学将铁与水蒸气高温反应后的固体物质溶解在过量盐酸中,如何判断所得溶液中是否含有Fe3+?
(1)将一定量的Fe粉、Cu粉、FeCl3溶液、CuCl2溶液混合于某容器中充分反应(假定容器不参与反应),判断下列情况下容器中金属离子与金属单质的存在情况:(用符号表示)
①若Fe粉有剩余,则容器中不可能有____________;
②若FeCl3有剩余,则容器中不可能有___________;
③若CuCl2有剩余,则容器中还可能有____________。
(2)有一瓶无色澄清溶液,可能含NH4+、K+、Na +、Mg2+、Ba2+、 Al3+、 Fe3+、SO42-、CO32-、Cl-、I-中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,表明溶液呈酸性;
②取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,CCl4层呈紫红色;
③取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
④取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:在溶液中肯定存在的离子有 ,肯定不存在的离子有 ,要确定是否存在的阴离子的实验方法是____________ 。