摘要:实例:
网址:http://m.1010jiajiao.com/timu_id_4024756[举报]
实验室里制取乙酸乙酯的主要步骤有:{1}在大试管中按一定比例配制乙酸、乙醇和浓硫酸的混合液 {2}小火加热试管内的混合液 {3}将产生的蒸气通入盛有饱和碳酸钠溶液的试管中.
试填写下列空白:
(1)配制乙酸、乙醇和浓硫酸的混合液的操作步骤是
(2)浓硫酸在这一反应中的作用是
(3)步骤{2}中采用小火加热的原因是
(4)步骤{3}中的主要注意事项是
查看习题详情和答案>>
试填写下列空白:
(1)配制乙酸、乙醇和浓硫酸的混合液的操作步骤是
先将乙酸和乙醇混合,然后将浓硫酸沿器壁缓缓倒入,并不断搅拌
先将乙酸和乙醇混合,然后将浓硫酸沿器壁缓缓倒入,并不断搅拌
;(2)浓硫酸在这一反应中的作用是
催化剂和吸水剂
催化剂和吸水剂
;(3)步骤{2}中采用小火加热的原因是
防止乙酸和乙醇的挥发
防止乙酸和乙醇的挥发
;(4)步骤{3}中的主要注意事项是
导管口不能伸入液面下
导管口不能伸入液面下
,因为防止因加热不匀发生倒吸
防止因加热不匀发生倒吸
.实验室制乙酸乙酯得主要装置如图中A所示,主要步骤①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;③小火加热a试管中的混合液;④等b试管中收集到约2mL产物时停止加热.撤下b试管并用力振荡,然后静置待其中液体分层;⑤分离出纯净的乙酸乙酯.

请回答下列问题:
(1)步骤①中,配制这一比例的混合液的正确操作是
(2)若实验中用含18O的乙醇与乙酸作用,该反应得化学方程式是:
(3)步骤③中,要用小火加热,其原因是
(4)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:
(5)A装置中使用球形管除起到冷凝作用外,另一重要作用是
(6)为充分利用反应物,甲、乙两位同学分别设计了图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).你认为合理的是
查看习题详情和答案>>

请回答下列问题:
(1)步骤①中,配制这一比例的混合液的正确操作是
在试管中加入3mL乙醇,然后边摇动边加入2mL浓硫酸和2mL乙酸;
在试管中加入3mL乙醇,然后边摇动边加入2mL浓硫酸和2mL乙酸;
.(2)若实验中用含18O的乙醇与乙酸作用,该反应得化学方程式是:
CH3COOH+CH3CH218OH
CH3CO18OC2H5+H2O
| 浓硫酸 |
| 加热 |
CH3COOH+CH3CH218OH
CH3CO18OC2H5+H2O
.| 浓硫酸 |
| 加热 |
(3)步骤③中,要用小火加热,其原因是
防止温度过高,乙酸乙醇挥发溢出;
防止温度过高,乙酸乙醇挥发溢出;
.(4)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:
2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑
2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑
.(5)A装置中使用球形管除起到冷凝作用外,另一重要作用是
防止倒吸;
防止倒吸;
,步骤⑤中分离乙酸乙酯必须使用的一种仪器是分液漏斗;
分液漏斗;
.(6)为充分利用反应物,甲、乙两位同学分别设计了图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).你认为合理的是
乙
乙
. 实验室合成乙酸乙酯时,得到乙酸乙酯粗产品.请回答下列问题:
实验室合成乙酸乙酯时,得到乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
(1)在烧瓶中除了加入
乙醇
乙醇
、浓硫酸
浓硫酸
、乙酸
乙酸
外,还应放入几块碎瓷片,其目的是防止烧瓶中液体暴沸.(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是:
先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡
先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡
.(3)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,当达到化学平衡状态时:(填序号)
②④⑤
②④⑤
.①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等 ⑤混合物中各物质的浓度不再变化
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图.请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法.

E为
乙醇
乙醇
(填名称);试剂a是饱和碳酸钠溶液
饱和碳酸钠溶液
,试剂b为浓硫酸
浓硫酸
;分离方法①是分液
分液
,分离方法②是蒸馏
蒸馏
.(5)写出合成乙酸乙酯反应的化学方程式
CH3COOH+C2H5OH
CH3COOC2H5+H2O
| 浓硫酸 |
| 加热 |
CH3COOH+C2H5OH
CH3COOC2H5+H2O
.| 浓硫酸 |
| 加热 |
实验室用如图所示装置可制取并探究SO2的性质

(1)A中盛放浓H2SO4的仪器名称是
(2)若B中盛放适量Na2S溶液,实验中出现淡黄色沉淀,说明SO2具有
(3)若探究SO2的还原性,可在C中盛放适量下例溶液中的
A.浓硫酸 B.溴水 C.酸性高锰酸钾溶液 D.氢氧化钡溶液
(4)若在D中盛放Ba(NO3)2溶液,发生反应的化学方程式为:
查看习题详情和答案>>

(1)A中盛放浓H2SO4的仪器名称是
分液漏斗
分液漏斗
,使用该仪器前必须进行的一步操作是检漏
检漏
;(2)若B中盛放适量Na2S溶液,实验中出现淡黄色沉淀,说明SO2具有
氧化性
氧化性
性;(3)若探究SO2的还原性,可在C中盛放适量下例溶液中的
BC
BC
;A.浓硫酸 B.溴水 C.酸性高锰酸钾溶液 D.氢氧化钡溶液
(4)若在D中盛放Ba(NO3)2溶液,发生反应的化学方程式为:
3Ba(NO3)2+3SO2+2H2O=3BaSO4+2NO+4HNO3
3Ba(NO3)2+3SO2+2H2O=3BaSO4+2NO+4HNO3
.实验室合成乙酸乙酯的步骤如下:在园底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
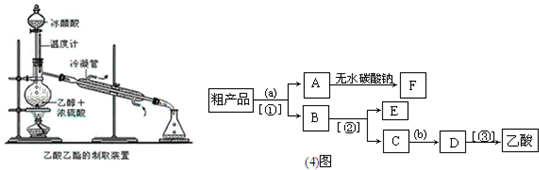
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是:
(3)在该实验中,若用1mol乙醇和1mol 乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯?
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图.请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法.试剂a是
(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是
(6)写出C→D 反应的化学方程式
查看习题详情和答案>>

(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是
防止烧瓶中液体暴沸
防止烧瓶中液体暴沸
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是:
先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡
先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡
.(3)在该实验中,若用1mol乙醇和1mol 乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯?
否
否
,原因是该反应是可逆反应,反应不能进行到底
该反应是可逆反应,反应不能进行到底
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图.请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法.试剂a是
饱和碳酸钠溶液
饱和碳酸钠溶液
,试剂b是浓硫酸
浓硫酸
;分离方法①是分液
分液
,分离方法②是蒸馏
蒸馏
,分离方法③是蒸馏
蒸馏
.(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是
除去乙酸乙酯中混有的少量水
除去乙酸乙酯中混有的少量水
(6)写出C→D 反应的化学方程式
2CH3COONa+H2SO4=Na2SO4+2CH3COOH
2CH3COONa+H2SO4=Na2SO4+2CH3COOH
.