网址:http://m.1010jiajiao.com/timu_id_4020982[举报]
| |||||||||||||||
根据化学实验仪器的特征和用途回答下列问题:
(1)下列仪器中,根据物质的沸点不同分离物质时需要的是(填编号)________.
①容量瓶 ②普通漏斗 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥滴定管 ⑦燃烧匙 ⑧温度计 ⑨干燥管
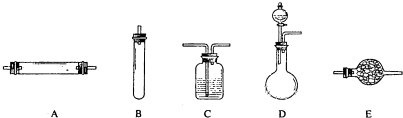
(2)实验室里不同化学试剂的保存方法不尽相同.下图中的A、B、C、D、E是常见的一些保存药品的试剂瓶.请把下列常见试剂的序号填写在各试剂瓶下面的括号内.
①NaOH溶液 ②浓硫酸 ③Na2CO3溶液 ④白磷 ⑤大理石 ⑥酒精 ⑦氯水 ⑧浓硝酸

(3)对于下列仪器,用序号回答有关问题:
①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
对允许加热的仪器,加热时必须垫石棉网的是________;使用时必须检查是否漏水的是________;标有“0”刻度的有________.
(10分)N2在诸多领域用途广泛。某化学兴趣小组为探究在实验室制备较为纯净N2的方法,进行了认真的准备。请你参与交流与讨论。
【查阅资料】 N2的制法有下列三种方案:
方案1:加热NaNO2和NH4Cl的浓溶液制得N2。
方案2:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉。
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2。
【实验准备】以实验室常见仪器(药品)等设计的部分装置如下图(有的夹持和加热仪器未画出)。
【分析交流】

⑴若以方案1制得N2,应选择的发生装置是 。
⑵若按方案2制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的顺序连接的顺序是(填写序号,下同) 。获得N2的反应原理是(写反应方程式) 。
⑶若以排水法收集N2,其中会混入水蒸气。但也不宜用排空气法,其原因是 。你提出的收集方法是 。
⑷上述三个方案中,制得的N2纯度最差的是 。在N2纯度要求不甚严格的情况下,有人建议将方案2和方案3结合使用,你认为其优点是 。
查看习题详情和答案>>方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气.进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置
(选填装置编号)中加入
(3)方法三:制氮气的化学方程式为:
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂.在制取氮气的3种方法中,联合使用方法-和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:
(5)1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右.若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:
实验室可通过多条途径得到氮气,常见的三种方法是:
方法一:将氨气通过灼热的氧化铜粉末,得到纯净的氮气和铜。
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末。
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,逸出氮气。
下列是进行实验时可选择的实验仪器(其它必要的仪器如:铁架台、铁夹、铁圈、石棉网、
酒精灯等未列出):
请回答下列问题:
(1)方法一制氮气:氨气是用浓氨水跟生石灰反应得到,此反应最好选用(填仪器的编号)
_________作发生装置,该反应的化学方程式_________________________。
要制取并收集纯净的氮气(可含有少量的水),还应使用上述仪器中的(填仪器的编号,
并按气流方向从左向右列出)_______________________________________________。
(2)制取氮气的三种方法中,方法一和方法二越来越受到人们的关注,经常被联合使用。
这两种方法与方法三相比,其优越性在于①____________ ______________________,
②_________________________________________。(至少写两点)
