摘要:答案. (2)2NaCl + 2H2O 2NaOH + H2↑ + Cl2↑ (3)Fe元素的化合价显+6价.易得电子 (6)KNO3 KCl. KNO3可用于化肥.炸药等
网址:http://m.1010jiajiao.com/timu_id_4016396[举报]
(2012?保定一模)【化学一化学与技术】
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如图:
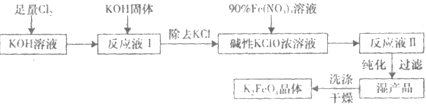
已知:
①温度较低时,Cl2通入KOH溶液生成次级酸盐;温度较高时,Cl2通入KOH溶液生成氯酸盐;
②Fe(NO3)3溶液与KClO溶液在强碱性环境中生成K2FeO4.请回答下列问题:
(1)该生产工艺应在
(2)为了提高生活用水的卫生标准,自来水厂常使用高铁酸钾(K2FeO4)进行消毒、净化以改善水质,其原因是
(3)经过高铁酸钾(K2FeO4)处理后的水不是纯净水,若要得到纯净水.可采用的净化方法是
(4)高铁酸钾溶于水形成浅紫红色溶液,溶液静置时会逐渐生成氧气并沉淀出三氧化二铁,此过程也会使溶液的pH增大.写出其化学方程式:
(5)在“反应液I”中加KOH固体的目的是为了①吸收“反应液I”中过量的Cl2,生成更多的KClO;②
(6)从“反应液Ⅱ”中分离出K2FeO4后,副产品是
查看习题详情和答案>>
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如图:

已知:
①温度较低时,Cl2通入KOH溶液生成次级酸盐;温度较高时,Cl2通入KOH溶液生成氯酸盐;
②Fe(NO3)3溶液与KClO溶液在强碱性环境中生成K2FeO4.请回答下列问题:
(1)该生产工艺应在
温度较低
温度较低
(填“温度较高”或“温度较低”)的情况下进行.(2)为了提高生活用水的卫生标准,自来水厂常使用高铁酸钾(K2FeO4)进行消毒、净化以改善水质,其原因是
+6价的Fe元素易得电子表现出强氧化性,可杀菌消毒,还原产物Fe元素为+3价,在水中形成Fe(OH)3胶体,可吸附水中悬浮物并可使泥沙聚沉
+6价的Fe元素易得电子表现出强氧化性,可杀菌消毒,还原产物Fe元素为+3价,在水中形成Fe(OH)3胶体,可吸附水中悬浮物并可使泥沙聚沉
(3)经过高铁酸钾(K2FeO4)处理后的水不是纯净水,若要得到纯净水.可采用的净化方法是
蒸馏
蒸馏
(4)高铁酸钾溶于水形成浅紫红色溶液,溶液静置时会逐渐生成氧气并沉淀出三氧化二铁,此过程也会使溶液的pH增大.写出其化学方程式:
4K2FeO4+4H2O=2Fe2O3+8KOH+3O2↑
4K2FeO4+4H2O=2Fe2O3+8KOH+3O2↑
(5)在“反应液I”中加KOH固体的目的是为了①吸收“反应液I”中过量的Cl2,生成更多的KClO;②
为下一步反应提供反应物
为下一步反应提供反应物
.(6)从“反应液Ⅱ”中分离出K2FeO4后,副产品是
KNO3
KNO3
和KCl
KCl
(写化学式).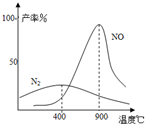 (2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下:
(2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下: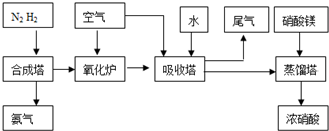
(1)某温度下体积为200L的氨合成塔中,测得如下数据:
| 时间(h)浓度(mol/L) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0 | 0.200 | 0.600 | C3 | C3 |
0.15
0.15
mol?L-1?h-1若起始时与平衡时的压强之比为a,则N2的转化率为
2(1-
)
| 1 |
| a |
2(1-
)
(用含a的代数式表示)| 1 |
| a |
(2)希腊阿里斯多德大学的 George Marnellos 和 Michael Stoukides,发明了一种合成氨的新方法(Science,2,Oct.1998,p98),在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式
N2+6H++6e-═2NH3
N2+6H++6e-═2NH3
(3)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
4NH3+5O2?4NO+6H2O K1=1×1053(900℃)
4NH3+3O2?2N2+6H2O K2=1×1067(900℃)温度较低时以生成
N2
N2
为主,温度高于900℃时,NO产率下降的原因生成NO的反应为放热反应,升高温度转化率下降
生成NO的反应为放热反应,升高温度转化率下降
.吸收塔中需要补充空气的原因进一步与NO反应生成硝酸
进一步与NO反应生成硝酸
.(4)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NOx的去除率高达99.95%.其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素反应生成CO2和N2请写出有关反应化学方程式
NO+NO2+H2O=2HNO2
NO+NO2+H2O=2HNO2
,CO(NH2)2+2HNO2=CO2+2N2+3H2O
CO(NH2)2+2HNO2=CO2+2N2+3H2O
.Na2CO3和NaHCO3是工业和生活中常见的物质.
(1)从组成上看,Na2CO3和NaHCO3都属于盐类,其共同特点使它们具有一些相似的性质.如:都能与
(2)观察是化学学习的重要方法.某同学在两支试管里分别加入各约1g Na2CO3和NaHCO3,仅用蒸馏水、酚酞、试管和玻璃棒,设计三种方法区分它们.下表是其观察记录,请你帮助完成.
查看习题详情和答案>>
(1)从组成上看,Na2CO3和NaHCO3都属于盐类,其共同特点使它们具有一些相似的性质.如:都能与
HCl
HCl
(填化学式)反应.(2)观察是化学学习的重要方法.某同学在两支试管里分别加入各约1g Na2CO3和NaHCO3,仅用蒸馏水、酚酞、试管和玻璃棒,设计三种方法区分它们.下表是其观察记录,请你帮助完成.
| 观察要点或实验步骤 | 现象、结论或注意事项 | |
| 方法一 | 观察二者外观上的细小差别 | 呈 白色粉末 白色粉末 状的是碳酸钠,呈白色细小晶体 白色细小晶体 的是碳酸氢钠 |
| 方法二 | 分别滴入几滴水 | 结成块状并且试管底部温度较高的是 碳酸钠 碳酸钠 ;未结块并且试管底部温度较低的是 碳酸氢钠 碳酸氢钠 . |
| 方法三 | 再分别加入10mL水,滴入 1~2滴酚酞试液 |
该操作中加入水后应 用力振荡或用玻璃棒搅拌 用力振荡或用玻璃棒搅拌 ;滴入酚酞后应着重观察 所得溶液颜色的深浅 所得溶液颜色的深浅 . |
(2011?湛江二模)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下:

(1)反应①应在温度较低的情况下进行.因在温度较高时KOH 与Cl2 反应生成的是KClO3.写出在温度较高时KOH 与Cl2反应的化学方程式
(2)在溶液I中加入KOH固体的目的是
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(4)如何判断K2FeO4晶体已经洗涤干净
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
FeO42-+H2O=Fe(OH)3(胶体)+O2↑+OH-.
查看习题详情和答案>>

(1)反应①应在温度较低的情况下进行.因在温度较高时KOH 与Cl2 反应生成的是KClO3.写出在温度较高时KOH 与Cl2反应的化学方程式
6KOH+3Cl2
KClO3+5KCl+3H2O
| ||
6KOH+3Cl2
KClO3+5KCl+3H2O
,该反应的氧化产物是
| ||
KClO3
KClO3
.(2)在溶液I中加入KOH固体的目的是
AC
AC
(填编号).A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
.(4)如何判断K2FeO4晶体已经洗涤干净
用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净.
用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净.
.(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
FeO42-+H2O=Fe(OH)3(胶体)+O2↑+OH-.
(2009?沈阳三模)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下:

已知:①2KOH+Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)该生产工艺应在
(2)写出工业上制取Cl2的化学方程式
(3)K2FeO4具有强氧化性的原因
(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度为
(5)在“反应液I”中加KOH固体的目的是
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品
查看习题详情和答案>>

已知:①2KOH+Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)该生产工艺应在
温度较低
温度较低
(填“温度较高”或“温度较低”)情况下进行;(2)写出工业上制取Cl2的化学方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
;
| ||
(3)K2FeO4具有强氧化性的原因
K2FeO4中铁元素化合价为+6价,易得电子
K2FeO4中铁元素化合价为+6价,易得电子
;(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度为
10mol/L
10mol/L
;(5)在“反应液I”中加KOH固体的目的是
AC
AC
:A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品
KNO3、KCl
KNO3、KCl
(写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途KNO3可用于化肥,炸药等
KNO3可用于化肥,炸药等
.