网址:http://m.1010jiajiao.com/timu_id_4009937[举报]
①提出假设:
假设Ⅰ:若过氧化钠氧化二氧化氮(反应只生成一种盐),则发生反应:
假设Ⅱ:若二氧化氮氧化过氧化钠(反应生成一种盐和一种气体单质),则发生反应:
②查阅资料:a.亚硝酸钠在酸性条件下能发生自身氧化还原反应:2NaNO2+2HCl═2NaCl+H2O+NO2↑+NO↑;
b.检验NO
- 3 |
- 3 |
| ||
③设计实验:
a.在一瓶集气瓶里充满红棕色的二氧化氮,用药匙放进一勺淡黄色的过氧化钠粉末,盖上毛玻璃片用力振荡,用手摸瓶壁感觉发烫,红棕色迅速消失了;
b.反应完后,用带火星的木条伸入瓶内,木条不复燃;
c.向反应后的残余物中加入盐酸,无明显现象;
d.将瓶内固体充分溶解,浓缩,再加入浓硫酸和铜粉共热,可产生红棕色有刺激性气味的气体,且溶液呈蓝色.
④实验结论:假设
B、已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验.
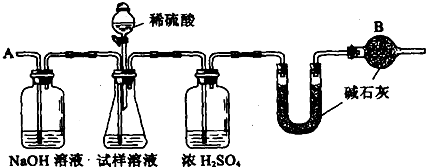
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到b g
④从分液漏斗滴入6mol?L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到c g
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为d g
请填空和回答问题:
(1)装置中干燥管B的作用是
(2)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果
(3)步骤⑤的目的是
(4)步骤⑦的目的是
(5)该试样中纯碱的质量分数的计算式为
| 106(d-b) |
| 44a |
| 106(d-b) |
| 44a |
铁是自然界里分布最广的金属元素之一,在地壳中的质量约占5%左右.铁矿石的种类很多,重要的有磁铁矿石(主要成分是 )、赤铁矿石(主要成分是
)、赤铁矿石(主要成分是 )等.
)等.
(1)写出赤铁矿炼铁的主要化学方程式____________________________.
(2)红热的铁能跟蒸气起反应,有一种产物是可燃气体,则其化学方程式为___________________________________________________________.
(3)在常温下,铁水不起反应,但是,在水和空气里的氧气及二氧化碳等的共同作用下,铁很容易生锈而被腐蚀,每年因腐蚀损失的钢材占世界钢铁年产量的四分一,刷油漆是重要的防腐蚀的措施之一,油漆防腐蚀的主要原因是________________________________________________.
(4)铁元素是人的重要营养元素,举例说明铁元素在人体中的重要作用:_____________________________________________________________.
(5)富有经验的工在向木器钉铁打时,习惯用口水把铁钉尖部湿润,然后钉入木器,其目的有两个:一是___________________;二是_____________________________________________________________.
(6)已知 与
与 能形成稳定的配合离子
能形成稳定的配合离子 .硫酸亚铁可用于治疗缺铁性贫血,而硫酸铁无此药效.硫酸亚铁药片外表包有一层特制的糖衣,该糖的作用是_______________________________________________.并简述如何用实验方法来检验某硫酸亚铁药片是否变质(即是否含
.硫酸亚铁可用于治疗缺铁性贫血,而硫酸铁无此药效.硫酸亚铁药片外表包有一层特制的糖衣,该糖的作用是_______________________________________________.并简述如何用实验方法来检验某硫酸亚铁药片是否变质(即是否含 )?是部分质还是全部变质?
)?是部分质还是全部变质?
 Ca2++2OH-.加入以下溶液,可使Ca(OH)2减少的是( )
Ca2++2OH-.加入以下溶液,可使Ca(OH)2减少的是( )