摘要:6.MgCl2形成过程: + Mg + Mg2+ 四十三.原电池:
网址:http://m.1010jiajiao.com/timu_id_400918[举报]
1808年,英国化学家戴维用钾还原氧化镁,最早制得少量的镁.镁是航空工业的重要材料,镁合金用于制造飞机机身、发动机零件等,一架超音速飞机约有5%的镁合金构件,一枚导弹一般消耗100~200公斤镁合金;镁作为一种强还原剂,还用于钛、锆、铍和铀等的生产中;镁是燃烧弹和照明弹不能缺少的组成物;镁粉是节日烟花必需的原料.镁及其合金是一种用途很广泛的金属材料,目前世界上60%的镁是从海水中提取的.从海水(主要含NaCl和MgSO4)中提取金属镁的主要步骤如图:
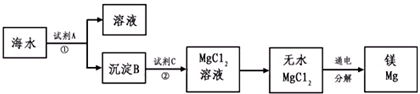
回答下列问题:
(1)Mg在周期表中的位置 ,试剂A可以选用 ,试剂C可选用 ;
(2)步骤①的离子方程式 ;
(3)用电子式表示氯化镁的形成过程 ;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为: ;
(5)戴维制镁的化学方程式为 ;
(6)配平下列反应的方程式.
①UF4+Mg--U+MgF2
②Mg+HNO3--Mg(NO3)2+N2O↑+H2O. 查看习题详情和答案>>

回答下列问题:
(1)Mg在周期表中的位置
(2)步骤①的离子方程式
(3)用电子式表示氯化镁的形成过程
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:
(5)戴维制镁的化学方程式为
(6)配平下列反应的方程式.
①UF4+Mg--U+MgF2
②Mg+HNO3--Mg(NO3)2+N2O↑+H2O. 查看习题详情和答案>>
1808年,英国化学家戴维用钾还原氧化镁,最早制得少量的镁。镁是航空工业的重要材料,镁合金用于制造飞机机身、发动机零件等,一架超音速飞机约有5%的镁合金构件,一枚导弹一般消耗100~200公斤镁合金;镁作为一种强还原剂,还用于钛、锆、铍和铀等的生产中;镁是燃烧弹和照明弹不能缺少的组成物;镁粉是节日烟花必需的原料。镁及其合金是一种用途很广泛的金属材料,目前世界上60%的镁是从海水中提取的。从海水(主要含NaCl和MgSO4)中提取金属镁的主要步骤如下:

回答下列问题:
(1)Mg在周期表中的位置______________________,试剂A可以选用_____________________,试剂C可选用_______________________;
(2)步骤①的离子方程式_________________________________________;
(3)用电子式表示氯化镁的形成过程_______________________________;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:_____________________________________________________;
(5)戴维制镁的化学方程式为_____________________________________;
(6)配平下列反应的方程式。
①  +
+  ——
——
 +
+ 
②  +
+  ——
——
 +
+  +
+

查看习题详情和答案>>
Mg及其化合物可以发生如下转化(部分反应物、生成物或水已略去),已知X、Y、Z为气态单质,B常温下为液态,D的焰色为黄色,C和G混合冒白烟并生成A。

(1)写出下列物质的化学式:A________;Y________。
(2)请用电子式表示B的形成过程:________________________。
(3)请用电离或水解平衡解释A+B+Mg→C+X+MgCl2的原因__________________
(4)将1 molCO2通入1L溶质为F的溶液中,充分反应后,再向混合液中逐滴滴加盐酸,所加盐酸的体积与生成的气体的关系如下图所示,原F溶液的物质的量浓度为___________mol/L。
(2)请用电子式表示B的形成过程:________________________。
(3)请用电离或水解平衡解释A+B+Mg→C+X+MgCl2的原因__________________
(4)将1 molCO2通入1L溶质为F的溶液中,充分反应后,再向混合液中逐滴滴加盐酸,所加盐酸的体积与生成的气体的关系如下图所示,原F溶液的物质的量浓度为___________mol/L。

按要求书写电子式。
a.原子电子式的书写:H____;Mg____;Al______; C______;N____;O____; F____;Ne_____;
b.简单阳离子电子式的书写:钠离子______;镁离子______;铝离子______;氢离子______;
c.简单阴离子电子式的书写:硫离子______;氯离子______;氧离子______; 氢负离子______;
d.离子化合物的电子式书写:MgO_______,Na2S_______ K2S:_______;CaF2_______;
e.用电子式表示离子键的形成过程:KBr_______;MgCl2_______;K2O_______
查看习题详情和答案>>
a.原子电子式的书写:H____;Mg____;Al______; C______;N____;O____; F____;Ne_____;
b.简单阳离子电子式的书写:钠离子______;镁离子______;铝离子______;氢离子______;
c.简单阴离子电子式的书写:硫离子______;氯离子______;氧离子______; 氢负离子______;
d.离子化合物的电子式书写:MgO_______,Na2S_______ K2S:_______;CaF2_______;
e.用电子式表示离子键的形成过程:KBr_______;MgCl2_______;K2O_______
下表中数据是第三周期的三种金属元素X、Y、Z逐渐失去电子的电离能.
试回答下列问题
(1)根据数据分析,X、Y、Z的最外层电子数,简述理由
(2)X元素的原子核外最外层电子排布式为
(3)X、Y、Z三元素的原子半径由大到小顺序为
(4)第三周期中能与Y元素形成YD型化合物的元素D位于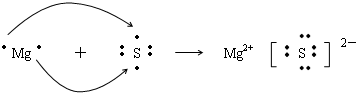
 .
.
(5)写出金属Y与石墨电极、稀硫酸构成的原电池的电极反应式:
负极:
正极:
查看习题详情和答案>>
| 电离能/kJ?mol-1 | |||||||
| X | 578 | 1817 | 2745 | 11575 | 14830 | 18376 | 23293 |
| Y | 738 | 1451 | 7733 | 10540 | 13630 | 17995 | 21703 |
| Z | 496 | 4562 | 6912 | 9943 | 13353 | 16610 | 20114 |
(1)根据数据分析,X、Y、Z的最外层电子数,简述理由
X、Y、Z的最外层电子数分别是3、2、1,由电离能相差很大时较小的电离能即为其最外层电子全失去时的电离能,从而确定其最外层电子数
X、Y、Z的最外层电子数分别是3、2、1,由电离能相差很大时较小的电离能即为其最外层电子全失去时的电离能,从而确定其最外层电子数
.(2)X元素的原子核外最外层电子排布式为
3s23p1
3s23p1
.(3)X、Y、Z三元素的原子半径由大到小顺序为
Z>Y>X(或Na>Mg>Al)
Z>Y>X(或Na>Mg>Al)
;X、Y、Z三元素的离子半径由大到小顺序为Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+)
Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+)
.(4)第三周期中能与Y元素形成YD型化合物的元素D位于
ⅥA
ⅥA
族,用电子式表示化合物YD的形成过程

(5)写出金属Y与石墨电极、稀硫酸构成的原电池的电极反应式:
负极:
Mg-2e-═Mg2+
Mg-2e-═Mg2+
正极:
2H++2e-═H2↑
2H++2e-═H2↑
.