网址:http://m.1010jiajiao.com/timu_id_400741[举报]
请回答以下问题:
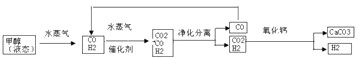
(1)液态甲醇雾化后与水蒸气混合,其目的是
(2)为了测定CH3OH(g)+H2O(g)→CO2(g)+3H2(g)的反应速率,在某温度下用气体传感器测得不同时间的甲醇和水蒸气浓度如下:
| 时间 s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(CH3OH) /mol.L-1 |
1.00×10-3 | 4.50×10-4 | 2.5 0×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| C(H2O) mol.L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.7×10-3 | 2.7×10-3 |
②在该温度下,反应的平衡常数表达式K=
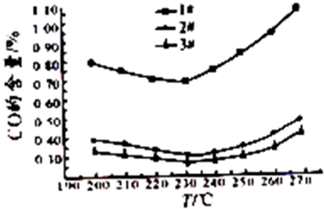
(3)为了研究反应条件对CO含量的影响,在甲醇含量为50%,原料液进料量60mL/h的情况下,在常压下和在不同催化环境下得到了反应温度与CO含量的关系图.从图中得到的有关结论是
(4)为研究反应中压强对CO含量的影响,请简述你的实验方案:

①已知:①2RCOO-
| 电解 |
②化合物A能与FeCl3溶液发生显色反应,但不与溴水反应,其苯环和侧链烃基上的一取代物均只有一种.③副产物H中有3个六元环,红外光谱测试,其分子中不含甲基,H-NMR谱显示其含有5种化学环境不同的氢原子,且个数比为1:2:2:2:1.根据以上信息回答下列问题.
(1)下列叙述正确的是
A.X属卤代芳烃 B.A分子中含有多苯代脂结构单元
C.化合物I可以和Na2CO3溶液反应,放出CO2气体 D.化合物B可发生缩聚反应
(2)写出J的名称
(3)写出同时满足下列条件的E的所有同分异构体的结构简式(不考虑立体异构)
a.含苯环但不含甲基 b.属于酯类 c.能发生银镜反应
(4)写出F→G反应的化学方程式
(5)写出B→H反应的化学方程式
氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g) ![]() 2NH3(g);ΔH = -92.2 kJ·mol-1。
2NH3(g);ΔH = -92.2 kJ·mol-1。
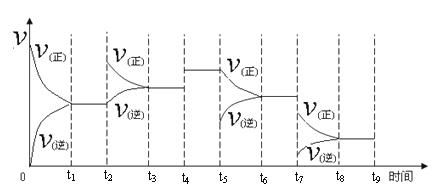
一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻所对应的实验条件改变分别是
t4 t5 t7 。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g) ![]() H2(g) + CO(g) △H = +131.3 kJ/mol
H2(g) + CO(g) △H = +131.3 kJ/mol
①该反应在低温下不能自发进行的原因是 。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度 ( )
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol碘化氢(a>b)待反应:2HI(g)![]() H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
(9分)氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g) 2NH3(g);ΔH = -92.2 kJ·mol-1。
①一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t2 ﹑t4 ﹑t5 ﹑t7时刻所对应的实验条件改变分别是
t2 t4 t5 t7 。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入1mol及2mol碘化氢待反应:2HI(g)H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
查看习题详情和答案>>
氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g)+ 3H2(g) 2NH3(g);ΔH= -92.2 kJ·mol-1。
① 一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻所对应的实验条件改变分别是
t4 t5 t7 。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g) H2(g)+ CO(g) △H = +131.3 kJ/mol
①该反应在低温下不能自发进行的原因是 。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度 ( )
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol碘化氢(a>b)待反应:2HI(g)H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
查看习题详情和答案>>