摘要:9]硫酸铵是农村常用的一种铵态氮肥.试回答下列问题: ⑴某硫酸铵肥料.实验测得氮的质量分数为20%.这种样品中可能混有( ). A.碳酸氢铵 B.硝酸铵 C.氯化铵 D.磷酸氢二铵 ⑵下列物质不能跟硫酸铵肥料混合施用的是( ). A.碳酸氢铵 B.草木灰 C.过磷酸钙 D.氯化钾 ⑶田间一次施用化肥过多会使植物变得枯萎发黄.俗称“烧苗 .其原因是( ). A.根细胞从土壤中吸收的养分过多 B.根细胞不能从土壤中吸水 C.根系不能将水向上运输 D.根系加速了呼吸作用.释放的能量过多 [命题解读]要求“了解化学肥料.农药等在农业生产中的作用. 本题以最常见的氮肥硫酸铵为材料考查了学生对化肥知识的掌握情况.涉及到了计算.化肥的施用过程中易出现的问题等多方面的知识.对学生综合应用知识的能力要求很高.这一类题一般难度不大.往往以生活常识为背景.有新意. [解题指导]⑴硫酸铵含氮量为21.2%>20%.则必定含有含氮量比20%小的一种化肥.经计算只有NH4HCO3含氮量低于20%. ⑵硫酸铵为铵态氮肥.这种肥料不能跟碱性物质混合使用.因易产生挥发物质氨气.降低肥效.而草木灰的主要成分是K2CO3.水解显碱性. ⑶当使用化肥过多时.根细胞不能从土壤中吸水而发黄. 答案:⑴A ⑵B ⑶B
网址:http://m.1010jiajiao.com/timu_id_4004585[举报]
氮肥是广泛使用的肥料,请结合有关材料,回答问题.
(1)硫酸铵是农村常用的一种铵态氮肥.
①硫酸铵中氮的质量分数是__________.
②实验测得某硫酸铵肥料中氮元素的质量分数为20%,则该样品中可能混有_____________.
[ ]
A.碳酸氢铵
B.硝酸铵
C.氯化铵
D.磷酸氢二铵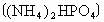
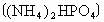
(2)电闪雷鸣是日常生活中司空见惯的现象.在闪电发生的过程中,空气中的氮气和氧气直接化合.假设某次雷电放出的能量为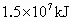 ,已知
,已知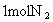 和
和 化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
①此次闪电所产生的NO的物质的量是_____mol.
②此次雷电的生成物相当于给土壤施加了_______千克的尿素化肥〔尿素化学式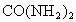 〕.
〕.
氮肥是广泛使用的肥料,请结合有关材料,回答问题.
(1)硫酸铵是农村常用的一种铵态氮肥.
①硫酸铵中氮的质量分数是__________.
②实验测得某硫酸铵肥料中氮元素的质量分数为20%,则该样品中可能混有_____________.
[ ]
A.碳酸氢铵
B.硝酸铵
C.氯化铵
D.磷酸氢二铵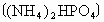
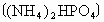
(2)电闪雷鸣是日常生活中司空见惯的现象.在闪电发生的过程中,空气中的氮气和氧气直接化合.假设某次雷电放出的能量为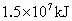 ,已知
,已知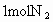 和
和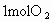 化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
①此次闪电所产生的NO的物质的量是_____mol.
②此次雷电的生成物相当于给土壤施加了_______千克的尿素化肥〔尿素化学式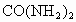 〕.
〕.
硫酸铵是一种常用的铵态氮肥.下表是硫酸铵化肥品质的主要指标.?
某化学研究性学习小组为本地农业生产服务,对某农用品商店出售的一等品硫酸铵化肥的品质进行探究 .?
.?
[观察外观]
该硫酸铵化肥无可见机械杂质.?
[实验探究]
按如图所示装置进行实验.?
(1)烧瓶内发生反应的离子方程式为:
(2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是
[交流讨论]
甲同学:根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:
乙同学:实验装置中还存在另一个明显缺陷是:
经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验
[探究结论]
称取13.5g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验后B装置增重3.4g.得出探究结论为
查看习题详情和答案>>
| 指标 项目 |
优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |
 .?
.?[观察外观]
该硫酸铵化肥无可见机械杂质.?
[实验探究]
按如图所示装置进行实验.?
(1)烧瓶内发生反应的离子方程式为:
NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
烧杯中盛放的试剂最好是
| ||
稀硫酸
稀硫酸
(填“浓硫酸”、“稀硫酸”或“水”)(2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是
使硫酸铵充分反应完全转化为NH3
使硫酸铵充分反应完全转化为NH3
[交流讨论]
甲同学:根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:
A、B装置间缺一个干燥装置
A、B装置间缺一个干燥装置
乙同学:实验装置中还存在另一个明显缺陷是:
缺少赶尽反应装置中残留氨气的装置
缺少赶尽反应装置中残留氨气的装置
经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验
[探究结论]
称取13.5g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验后B装置增重3.4g.得出探究结论为
该化肥为合格品
该化肥为合格品
.下图为某些常见物质之间的转化关系.已知:A、B、I中含有相同的阳离子且都是XY2型化合物,且I是实验室常用的干燥剂;C为直线型分子;E、F为非金属气体单质.
请按要求填空:

(1)①B的电子式是
 ,②K的结构式是
,②K的结构式是
(2)D与G反应的化学方程式是
(3)已知C的燃烧热是1300kJ/mol,表示C的燃烧热的热化学方程式是
(4)将G溶于水配成溶液,简述检验该溶液G中所含阳离子的操作方法:
(5)常温下0.1mol/L的J溶液中c(H+)/c(OH-)=1×10-8,下列叙述错误的是
A.该溶液的pH=11;
B.该溶液中的溶质电离出的阳离子浓度0.1mol/L
C.该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-22
D.pH=3的盐酸溶液V1 L与该0.1mol/L的J溶液V2 L混合,若混合溶液pH=7,则:V1>V2
E.将以上溶液加水稀释100倍后,pH值为9;
(6)单质F在工业上有重要的用途是
查看习题详情和答案>>
请按要求填空:

(1)①B的电子式是


H-O-Cl
H-O-Cl
;(2)D与G反应的化学方程式是
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
;
| ||
(3)已知C的燃烧热是1300kJ/mol,表示C的燃烧热的热化学方程式是
C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol
| 5 |
| 2 |
C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol
;| 5 |
| 2 |
(4)将G溶于水配成溶液,简述检验该溶液G中所含阳离子的操作方法:
取少量的G溶液于试管中,加入适量的氢氧化钠溶液,加热试管,将湿润的红色石蕊试纸放在试管口,若试纸变成蓝色,则含有NH4+,(其他合理答案均给分)
取少量的G溶液于试管中,加入适量的氢氧化钠溶液,加热试管,将湿润的红色石蕊试纸放在试管口,若试纸变成蓝色,则含有NH4+,(其他合理答案均给分)
;(5)常温下0.1mol/L的J溶液中c(H+)/c(OH-)=1×10-8,下列叙述错误的是
BCE
BCE
;A.该溶液的pH=11;
B.该溶液中的溶质电离出的阳离子浓度0.1mol/L
C.该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-22
D.pH=3的盐酸溶液V1 L与该0.1mol/L的J溶液V2 L混合,若混合溶液pH=7,则:V1>V2
E.将以上溶液加水稀释100倍后,pH值为9;
(6)单质F在工业上有重要的用途是
制漂白粉,制盐酸(制漂白液等)
制漂白粉,制盐酸(制漂白液等)
.(至少两种)(1)保证食品安全、保持营养均衡,是人体健康的基础.
①餐饮业产生的“地沟油”的主要成分是油脂.一定条件下,油脂水解可以生成高级脂肪酸和
②若人体内缺乏铁元素,人就会患的疾病是缺铁性贫血,血液输送
③下列营养素中,不能对人体提供能量的是
A.维生素 B.糖类 C.蛋白质
④人体内缺乏某种维生素会引起坏血病,这种维生素是
⑤氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(-NH2)和
⑥淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),写出相应的化学方程式:
(2)下列是生活常用的物质:
A.碳酸氢钠 B.青霉素 C葡萄糖D.苯甲酸钠 E.柠檬黄
①可用作食品着色剂的是
②可直接进入血液补充能量的是
③可用作食品防腐剂的是
④属于抗生素的是
⑤治疗胃酸过多的是
(3)采取适当的措施能减少对环境的污染.
①对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为
②天然水中含有的细小悬浮颗粒可以用
查看习题详情和答案>>
①餐饮业产生的“地沟油”的主要成分是油脂.一定条件下,油脂水解可以生成高级脂肪酸和
甘油
甘油
.②若人体内缺乏铁元素,人就会患的疾病是缺铁性贫血,血液输送
氧
氧
的能力下降.③下列营养素中,不能对人体提供能量的是
A
A
.(填字母)A.维生素 B.糖类 C.蛋白质
④人体内缺乏某种维生素会引起坏血病,这种维生素是
维生素C
维生素C
(填“维生素A”或“维生素C”).⑤氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(-NH2)和
-COOH
-COOH
(写结构简式).人体中共有二十多种氨基酸,其中人体自身不能
不能
(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸.⑥淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),写出相应的化学方程式:
(C6H10O5)n+nH2O
nC6H12O6
| 催化剂 |
(C6H10O5)n+nH2O
nC6H12O6
.| 催化剂 |
(2)下列是生活常用的物质:
A.碳酸氢钠 B.青霉素 C葡萄糖D.苯甲酸钠 E.柠檬黄
①可用作食品着色剂的是
E
E
(填字母,下同);②可直接进入血液补充能量的是
C
C
;③可用作食品防腐剂的是
D
D
;④属于抗生素的是
B
B
;⑤治疗胃酸过多的是
A
A
.(3)采取适当的措施能减少对环境的污染.
①对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为
2NO+2CO
N2+2CO2
| ||
2NO+2CO
N2+2CO2
.
| ||
②天然水中含有的细小悬浮颗粒可以用
明矾(或聚合氯化铝或硫酸亚铁等)
明矾(或聚合氯化铝或硫酸亚铁等)
做混凝剂(写名称)进行净化处理.工业废水中含有的Cr3+离子,可用熟石灰作沉淀剂,在pH为8~9时生成沉淀而除去,该反应的离子方程式是Cr3++3OHˉ=Cr(OH)3↓
Cr3++3OHˉ=Cr(OH)3↓
.可用漂白粉对天然水进行消毒,漂白粉的有效成分是Ca(ClO)2
Ca(ClO)2
(填化学式).