网址:http://m.1010jiajiao.com/timu_id_400398[举报]
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因;
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等.
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容.
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(已知:MnO4_还原产物是Mn2+)
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是
(3)猜想Ⅱ可能是
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
| 试管A | 试管B | |
| 加入试剂 | ||
| (预期)实验现象 (褪色时间) |
||
| 结论 | 猜想Ⅱ正确 | |
(1)在当代人们的生活中,你所知道的利用太阳能辐射加热物体的方式有
(2)在生物质能的利用过程中,可以制得重要的有机物乙醇.某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇的组成元素的确定、分子式的确定、分子结构的确定.
(Ⅰ)他们决定用分析乙醇燃烧的产物来确定乙醇中含有C、H两种元素,简要说明他们的实验操作方法和现象:
①证明含有氢元素的实验操作方法和现象是
②证明含有碳元素的实验操作方法和现象是
(Ⅱ)用分析燃烧产物来证实乙醇中还含有氧元素时,需要取得一些实验数据,这些数据应该是
实验中他们可能会用到下列装置,请你将必需的相关装置的序号按从左到右排出合理的顺序(→表示气体的流向):
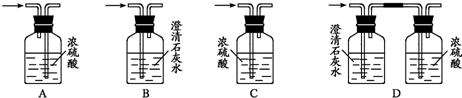
(Ⅲ)为确定乙醇的分子式,除(Ⅱ)中需要取得的数据外,你认为还是否需要测定乙醇的相对分子质量呢?
(Ⅳ)为确定乙醇的分子结构,他们先测定一定量无水乙醇和金属钠反应生成氢气的体积,选用了如下图所示的仪器装置(有的仪器配有双孔橡皮塞).则
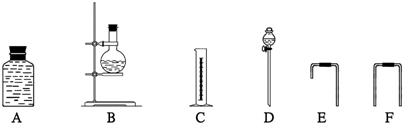
①这些仪器装置的合理的连接顺序是
②由实验证明乙醇的分子结构是CH3CH2OH而不是CH3OCH3的理由是
(3)开发新能源以缓解石油等的短缺引起的能源危机是一个重要课题.据报道,某地近年建设了一个年生产工业酒精500万吨的工厂,目的是为了将工业酒精与汽油混合作为汽车燃料而减少汽油的消耗量.已知生产酒精的方法有如下三种(用化学方程式表示):
方法一:CH2=CH2+H2O
| ||
| △ |
方法二:CH3-CH2Br+H2O
| ||
| △ |
方法三:(C6H10O5)n(淀粉)+n H2O
| 淀粉酶 |
C6H12O6(葡萄糖)
| 酒化酶 |
综合地看,你认为这三种方法中,较好的是
A.方法一 B.方法二 C.方法三
你认为该工厂生产工业酒精用的是
(10分)某校化学课外小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇的精制、乙醇组成元素的测定、分子式的测定、分子结构的测定。
(1)若所用乙醇中含少量水,采用直接蒸馏的方法不能有效除去水,通常向其中加入 ,然后蒸馏。证明乙醇不再含水,可用一种试剂检验,这种试剂是 。
(2)用燃烧乙醇分析产物的方法确定含有C、H、O三种元素。
a.证明含有H元素的操作是 。
b.证明含有O元素时,需取得的实验数据是:
CO2的质量,H2O的质量及 。
(3)为确定乙醇的分子式,在通过(2)获取乙醇的实验式之后,是否必须再测定乙醇的相对分子质量才能确定其分子式 (答“是”或“否”),理由是 。
(4)测定乙醇的分子结构
a.若采用红外光谱仪测定,则通过所得红外光谱中有 键的振动吸收峰,即可确定乙醇的结构是CH3CH2OH而不是CH3OCH3。(填“C—H”,“C—C”,“C—O”,“O—H”)
b.若采用核磁共振仪测定,则所得乙醇的核磁共振氢谱上应有 个吸收峰。
查看习题详情和答案>>
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大。小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等。
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容。
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(已知:MnO4_还原产物是Mn2+) 。
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是 。
(3)猜想Ⅱ可能是______________________________________________________________。要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是 。
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容。
|
|
试管A |
试管B |
|
加入试剂 |
|
|
|
(预期)实验现象 (褪色时间) |
|
|
|
结论 |
猜想Ⅱ正确 |
查看习题详情和答案>>
为节省药品和时间,甲、乙、丙三位同学用铜片、锌片、稀硫酸、CuSO4溶液;直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器(用品),以巧妙的构思,“接力”的方式,设计了比较铜与锌金属活泼性相对强弱的系列实验。试填写下列空白:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜、锌不接触),小心向烧杯中加入稀硫酸,观察到的现象是______________________________。甲同学的设计思路是________________________________________________________________________。
(2)乙同学接着甲的实验,向烧杯中滴加________溶液,进而观察到的现象是________________________________________________________________________,
________________________。乙同学判断出锌、铜金属活动性相对强弱所依据的原理是________________________________________________________________________
________________________________________________________________________,
________________________________________________________________________。
(3)丙同学使用直流电源和石墨电极组装电解装置,向乙同学实验后的溶液中补充了必要的试剂(作电解液)。反
应在调控下开始,有关电化学反应的化学方程式为______________________________。获得的明显实验现象是
________________________________________________________________________
________________________________________________________________________。
(4)请你再单独设计一个简单实验(试剂、仪器自选),证实锌和铜金属活泼性的相对强弱(简要说明操作步骤及现象)____________________________________
________________________________________________________________________
________________________________________________________________________。
查看习题详情和答案>>