摘要:(三)充分利用校内资源 校内课程资源包括校内的各种场所和设施.如图书馆.实验室.科普资料室.专用教室.信息中心等,校内人文资源.如教师群体特别是专家型教师.师生关系.班级组织.学生团体.校纪校风.校容校貌等,与教育教学密切相关的各种活动.如座谈讨论.文艺演出.化学晚会.社团活动.体育比赛.典礼仪式等.校内课程资源是实现课程目标.促进学生全面发展的最基本.最便利的资源.也最能引起我们的重视.其效果如何.关键在于我们能否以现代教育理念.根据学校自身特点.结合教学实际进行充分的挖掘和利用.
网址:http://m.1010jiajiao.com/timu_id_4002137[举报]
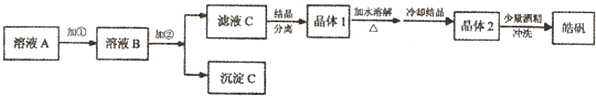
化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌.同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4?7H2O).某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾.制备皓矾的实验流程如图所示.

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)3:2.7-3.7Fe(OH)2:7.6-9.6 Zn(OH)2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用
(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)2,d、ZnCO3,e、ZnSO4等,可选用
(3)从晶体1→晶体2,该过程的名称是
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
查看习题详情和答案>>

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)3:2.7-3.7Fe(OH)2:7.6-9.6 Zn(OH)2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用
20%的H2O2
20%的H2O2
,其理由是将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
;(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)2,d、ZnCO3,e、ZnSO4等,可选用
bcd
bcd
;(3)从晶体1→晶体2,该过程的名称是
重结晶
重结晶
;(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
.(2009?宿迁二模)实验化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌.同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4?7H2O).某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾并探究其性质.
(1)制备皓矾的实验流程如图所示.
已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:
Fe(OH)3:2.7一3.7
Fe(OH)2:7.6一9.6
Zn(OH)2:5.7一8.0
试回答下列问题:①加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,应选用
②加入的试剂②,供选择使用的有:Zn粉、ZnO、Zn(OH)2、ZnCO3、ZnSO4等,应选用
③从晶体1→晶体2,该过程的名称是
④在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
(2)探究ZnSO4?7H2O的性质
⑤称取28.7g ZnSO4?7H2O研细后置于坩埚中小心加热,测得残留固体的质量与温度的对应数据见下表:
试写出ZnSO4?7H2O加热到1000℃时的反应方程式
⑥取少量ZnSO4?7H2O配成溶液向其中逐滴加入NaOH溶液,发现先产生白色沉淀后又逐渐溶解;若改用氨水得到相同的现象.查资料知,氢氧化锌与氢氧化铝均有两性,且锌离子可与氨水形成络合离子[Zn(NH3)4]2+.则Zn(OH)2沉淀中加入NaOH溶液和加氨水均得到无色溶液的离子反应方程式为:
查看习题详情和答案>>
(1)制备皓矾的实验流程如图所示.

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:
Fe(OH)3:2.7一3.7
Fe(OH)2:7.6一9.6
Zn(OH)2:5.7一8.0
试回答下列问题:①加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,应选用
20%的H2O2
20%的H2O2
,其理由是将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
②加入的试剂②,供选择使用的有:Zn粉、ZnO、Zn(OH)2、ZnCO3、ZnSO4等,应选用
ZnO、Zn(OH)2、ZnCO3
ZnO、Zn(OH)2、ZnCO3
,其理由是调节溶液PH到3.7,使铁离子沉淀,同时不引入新的杂质
调节溶液PH到3.7,使铁离子沉淀,同时不引入新的杂质
③从晶体1→晶体2,该过程的名称是
重结晶
重结晶
.④在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
.(2)探究ZnSO4?7H2O的性质
⑤称取28.7g ZnSO4?7H2O研细后置于坩埚中小心加热,测得残留固体的质量与温度的对应数据见下表:
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
ZnSO4?7H2O
ZnO+SO3+7H2O
| ||
ZnSO4?7H2O
ZnO+SO3+7H2O
.
| ||
⑥取少量ZnSO4?7H2O配成溶液向其中逐滴加入NaOH溶液,发现先产生白色沉淀后又逐渐溶解;若改用氨水得到相同的现象.查资料知,氢氧化锌与氢氧化铝均有两性,且锌离子可与氨水形成络合离子[Zn(NH3)4]2+.则Zn(OH)2沉淀中加入NaOH溶液和加氨水均得到无色溶液的离子反应方程式为:
Zn(OH)2+2OH-=ZnO22-+2H2O
Zn(OH)2+2OH-=ZnO22-+2H2O
(任写一个).(2013?浦东新区三模)重晶石矿(主要成分为硫酸钡)因为含有Fe2O3、MnO及炭质等杂质而常呈深褐色.工业上将重晶石矿粉碎后与硫酸、铝粉在反应槽中混合加热(即“漂白”),再经水洗等一系列工序制得白色的重晶石填料,广泛用作纸张、油漆等的填充剂.已知MnO是碱性氧化物,Al粉可以将深色的Fe3+转化为浅色的Fe2+.重晶石填料的生产工艺流程为:

(1)在该流程中,为加快“漂白”速度,采取的措施有
(2)硫酸起到了“漂白”的作用.请写出硫酸直接起到该作用时的化学方程式:
(3)二次漂白水洗过滤后,检验滤渣不含Fe2+离子的方法是
(4)二次漂白前,煅烧的主要目的是
(5)工业生产中为了充分利用资源,将滤液经过处理得到化工原料Fe2O3.操作过程是:
①滤液中通入过量Cl2,其目的是
②再加入适量NaOH来调节溶液的pH,其目的是
有关离子开始沉淀及完全沉淀时的pH如下:
(6)最后通过
查看习题详情和答案>>

(1)在该流程中,为加快“漂白”速度,采取的措施有
重晶石和铝都使用粉末
重晶石和铝都使用粉末
、加热
加热
.(2)硫酸起到了“漂白”的作用.请写出硫酸直接起到该作用时的化学方程式:
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
、MnO+H2SO4=MnSO4+H2O
MnO+H2SO4=MnSO4+H2O
.(3)二次漂白水洗过滤后,检验滤渣不含Fe2+离子的方法是
取最后一次洗涤液于试管中
取最后一次洗涤液于试管中
、先滴加氯水再滴加KSCN溶液无明显变化
先滴加氯水再滴加KSCN溶液无明显变化
.(4)二次漂白前,煅烧的主要目的是
除去炭质
除去炭质
.将煅烧后的固体磨成细粉,使用的是加有刚玉球的振动磨.这说明刚玉具有很高的硬度
硬度
.(5)工业生产中为了充分利用资源,将滤液经过处理得到化工原料Fe2O3.操作过程是:
①滤液中通入过量Cl2,其目的是
将Fe2+转化为Fe3+
将Fe2+转化为Fe3+
.②再加入适量NaOH来调节溶液的pH,其目的是
使Fe3+沉淀完全,而其它离子不发生沉淀
使Fe3+沉淀完全,而其它离子不发生沉淀
,调节溶液的pH范围为2.7-3.7
2.7-3.7
.有关离子开始沉淀及完全沉淀时的pH如下:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
洗涤干燥
洗涤干燥
、高温煅烧
高温煅烧
得到氧化铁.(2012?江苏一模)三聚磷酸钠(Na5P3O10)是一种优异的清洁剂添加剂.一种以黄磷(着火点40℃)为原料生产三聚磷酸钠的主要工艺如下:

(1)工业上黄磷放在铁桶中加水封盛装,其目的是
(2)在三聚磷酸钠的生产过程中,有大量的含磷废水产生,经过处理后才排放,其目的是
(3)上述工艺中,循环使用的物料除各种冷却水外,还有
(4)在中和釜中按计量比生成磷酸的两种酸式盐.这两种酸式盐在高温聚合时可生成三聚磷酸钠和另一种产物,该反应的化学方程式为
查看习题详情和答案>>

(1)工业上黄磷放在铁桶中加水封盛装,其目的是
防止黄磷在空气中氧化
防止黄磷在空气中氧化
;燃磷时,通入足量的空气,其目的是使黄磷充分氧化
使黄磷充分氧化
.(2)在三聚磷酸钠的生产过程中,有大量的含磷废水产生,经过处理后才排放,其目的是
减少磷资源流失(充分利用磷资源)
减少磷资源流失(充分利用磷资源)
;防止含磷废水引发水体富营养化(水体组成严重污染)
防止含磷废水引发水体富营养化(水体组成严重污染)
.(3)上述工艺中,循环使用的物料除各种冷却水外,还有
碳酸钠溶液
碳酸钠溶液
.(4)在中和釜中按计量比生成磷酸的两种酸式盐.这两种酸式盐在高温聚合时可生成三聚磷酸钠和另一种产物,该反应的化学方程式为
2Na2HPO4+NaH2PO4
Na5P3O10+10H2O
| ||
2Na2HPO4+NaH2PO4
Na5P3O10+10H2O
.
| ||