摘要:(三)卤素单质的化学性质 由于最外层均为 个电子.极易 电子.因此碱金属都是 剂.但随着电子层数递增.原子半径渐 .核对最外外层电子的引力渐 .失电子能力渐 .其还原性逐渐 . 试题枚举 [例1]:把小块金属钠分别投入饱和NaCl溶液.NH4Cl溶液.FeCl3的烧杯里的现象和反应? 现象 化学方程式 饱和NaCl 饱和NH4Cl FeCl3溶液
网址:http://m.1010jiajiao.com/timu_id_4001383[举报]
 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.(1)在光照条件下.氯气和氢气反应过程如下:
①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl …
反应②中形成的化合物的电子式为


非极性
非极性
键(填“极性”或“非极性”).(2)在短周期主族元素中,氯元素及与其相邻元素的原予半径从大到小的顺序是
S>Cl>F
S>Cl>F
.(用元素符号表示).与氯元素同周期且金属性最强的元素位于周期表的第
三
三
周期IA
IA
族.(3)卤索单质及化合物在许多性质上都存在着递变规律.下列有关说法正确的是
a
a
.a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b?卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c?卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d?卤索单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
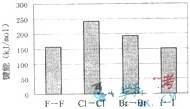
(4)卤素单质的键能大小如图.由图推断:
①非金属性强的卤素,其单质分子的化学键
不一定容易
不一定容易
断裂(填“容易”或“不容易”或“不一定容易”).②卤素单质键能大小与键长的关系为:
除F2外.键长增大,键能减小
除F2外.键长增大,键能减小
. X、Y、Z为三个不同短周期非金属元素的单质,在一定条件下有如下反应:Y+X![]() A(g),Y+Z
A(g),Y+Z![]() B(g)。
B(g)。
若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式是___________________。
②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是___________________。
③将Y与某卤素单质的水溶液充分反应可生成两种常见强酸,该反应的化学方程式是____________________________________________________________________________。
查看习题详情和答案>>
X、Y、Z为三个不同短周期非金属元素的单质,在一定条件下有如下反应:Y+X A(g),Y+Z
A(g),Y+Z B(g)。
B(g)。
若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式是___________________。
②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是___________________。
③将Y与某卤素单质的水溶液充分反应可生成两种常见强酸,该反应的化学方程式是__________________________________________________________________。
查看习题详情和答案>>