摘要:⑤中和法 例:H3C--OH + NaOH H3C--O Na +H2O
网址:http://m.1010jiajiao.com/timu_id_399996[举报]
(附加题) 工业上根据污水中所含物质或离子的不同,有多种处理方法,比如:
请回答:
(1)在中和法中,若用 CO2来处理污水,则离子方程式是
(2)在沉淀法中,用硫化钠作沉淀剂,能有效地处理含Cu2+、Hg2+等重金属离子的污水.若某污水中能与硫化钠反应的阳离子只有Hg2+,且含量为400mg/L,则处理10L这样的污水至少需要加入硫化钠
我国规定Hg2+ 的排放标准不能超过0.05mg/L,若1L污水经过沉淀法处理后含Hg2+为2×10-7mol,则该污水是否达到了排放标准
(3)在氧化还原法中,常用Cl2氧化污水中的有毒物质CN-,可得到无毒无害的CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式是
查看习题详情和答案>>
| 污水中所含离子 | 处理方法 |
| H+或OH- | 中和法 |
| Cu2+、Hg2+ | 沉淀法 |
| CN- | 氧化还原法 |
(1)在中和法中,若用 CO2来处理污水,则离子方程式是
CO2+OH-═HCO3-
CO2+OH-═HCO3-
.(2)在沉淀法中,用硫化钠作沉淀剂,能有效地处理含Cu2+、Hg2+等重金属离子的污水.若某污水中能与硫化钠反应的阳离子只有Hg2+,且含量为400mg/L,则处理10L这样的污水至少需要加入硫化钠
1.6
1.6
g(精确到0.1).我国规定Hg2+ 的排放标准不能超过0.05mg/L,若1L污水经过沉淀法处理后含Hg2+为2×10-7mol,则该污水是否达到了排放标准
是
是
(填“是”或“否”).(3)在氧化还原法中,常用Cl2氧化污水中的有毒物质CN-,可得到无毒无害的CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式是
5Cl2+2CN-+4H2O═10Cl-+2CO2+N2+8H+.
5Cl2+2CN-+4H2O═10Cl-+2CO2+N2+8H+.
.欲降低废水中重金属元素铬的毒性,可将Cr2O2-7转化为Cr(OH)3沉淀除去.
已知:
(1)某含铬废水处理的主要流程如图所示:
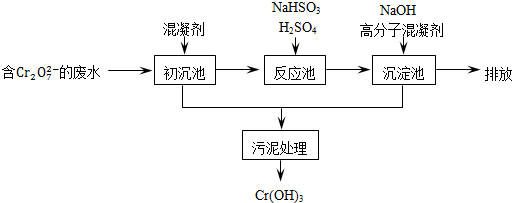
①沉池中加入的混凝剂是K2SO4?Al2(SO4)3?24H2O,用离子方程式表示其反应原理
②反应池中发生主要反应的离子方程式是Cr2O2-7+3HSO-3+5H+═2Cr3++3SO2-4+H2O.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是
(2)工业亦可用电解法来处理含Cr2O2-7废水.实验室利用如图模拟处理含Cr2O2-7的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-=H2↑.Fe2+与酸性溶液中的Cr2O2-7反应生成Cr3+和Fe3+,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是:
用电解法处理该溶液中0.01molCr2O2-7时,至少得到沉淀的质量是

查看习题详情和答案>>
已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | Fe2+ | 7.0 | 9.0 | Fe3+ | 1.9 | 3.2 | Cr3+ | 6.0 | 8.0 |

①沉池中加入的混凝剂是K2SO4?Al2(SO4)3?24H2O,用离子方程式表示其反应原理
Al3++3H2O?Al(OH)3(胶体)+3H+
Al3++3H2O?Al(OH)3(胶体)+3H+
.②反应池中发生主要反应的离子方程式是Cr2O2-7+3HSO-3+5H+═2Cr3++3SO2-4+H2O.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是
Cr3++3OH-═Cr(OH)3↓
Cr3++3OH-═Cr(OH)3↓
、H++OH-═H2O
H++OH-═H2O
.证明Cr3+沉淀完全的方法是测定溶液的pH,若pH≥8,则证明Cr3+沉淀完全
测定溶液的pH,若pH≥8,则证明Cr3+沉淀完全
.(2)工业亦可用电解法来处理含Cr2O2-7废水.实验室利用如图模拟处理含Cr2O2-7的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-=H2↑.Fe2+与酸性溶液中的Cr2O2-7反应生成Cr3+和Fe3+,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是:
阴极反应消耗了水中的H+,打破了水的电离平衡,促进了水的电离,使溶液中OH-浓度增大,溶液的碱性增强
阴极反应消耗了水中的H+,打破了水的电离平衡,促进了水的电离,使溶液中OH-浓度增大,溶液的碱性增强
.用电解法处理该溶液中0.01molCr2O2-7时,至少得到沉淀的质量是
8.48
8.48
g.
欲降低废水中重金属元素铬的毒性,可将Cr2O72-转化为Cr(OH)3沉淀除去.已知:
(1)某含铬废水处理的主要流程如图所示:
①初沉池中加入的混凝剂是K2SO4﹒Al2(SO4)3﹒24H2O,用离子方程式表示其反应原理是
②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+═2Cr3++3SO42-+4H2O.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是
(2)工业可用电解法来处理含 Cr2O72-废水.实验室利用如图模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-═H2↑.Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是
查看习题详情和答案>>
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cr3+ | 6.0 | 8.0 |

①初沉池中加入的混凝剂是K2SO4﹒Al2(SO4)3﹒24H2O,用离子方程式表示其反应原理是
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+═2Cr3++3SO42-+4H2O.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是
Cr3++3OH-═Cr(OH)3↓、H++OH-═H2O
Cr3++3OH-═Cr(OH)3↓、H++OH-═H2O
.证明Cr3+沉淀完全的方法是测定溶液的pH,若pH≥8,则证明Cr3+沉淀完全
测定溶液的pH,若pH≥8,则证明Cr3+沉淀完全
.
(2)工业可用电解法来处理含 Cr2O72-废水.实验室利用如图模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-═H2↑.Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是阴极反应消耗了水中的H+,打破了水的电离平衡,促进了水的电离,使溶液中OH-浓度增大,溶液的碱性增强
阴极反应消耗了水中的H+,打破了水的电离平衡,促进了水的电离,使溶液中OH-浓度增大,溶液的碱性增强
.用电解法处理该溶液中0.01mol Cr2O72-时,至少得到沉淀的质量是8.48
8.48
g.(11分)欲降低废水中重金属元素铬的毒性,可将Cr2O2-7转化为Cr(OH)3沉淀除去。已知:

(1)某含铬废水处理的主要流程如图所示:

①沉池中加入的混凝剂是K2SO4·Al2(SO4)3·24H2O,用离子方程式表示其反应原理
。
②反应池中发生主要反应的离子方程式是Cr2O2—7+3HSO—3+5H+===2Cr3++3SO2—4+H2O。根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是 、 。证明Cr3+沉淀完全的方法是 。
(2)工业亦可用电解法来处理含Cr2O2-7废水。实验室利用如图模拟处理含Cr2O2-7的废水,阳极反应式是Fe—2e—===Fe2+,阴极反应式是2H++2e—=H2↑。Fe2+与酸性溶液中的Cr2O2—7反应生成Cr3+和Fe3+,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是: 。
用电解法处理该溶液中0.01molCr2O2-7时,至少得到沉淀的质量是 g。

查看习题详情和答案>>