摘要:(1)上述系列中第1种物质的分子式为 .(2)以苯乙炔为基本原料.经过一定反应而得到最终产物.假设反应过程中原料无损失.理论上消耗苯乙炔与所得芳炔类大环化合物的质量比为 .
网址:http://m.1010jiajiao.com/timu_id_399932[举报]
物质A、B、C、D等的转化关系如图所示.已知A是由两种元素组成的化合物,B是常见的气态单质,J是常见的金属单质,H的相对分子质量比D大16(部分反应物、生成物未列出),反应①是工业上制取K的第一步反应,反应②为化合反应.

依据上述信息,回答下列的问题:
(1)J在元素周期表中的位置是 .
(2)F的水溶液显 (填“酸”、“碱”或“中”)性,用相关的离子方程式表示 .
(3)反应①的化学方程式为 .工业上反应①在 (填工业设备名称)中进行.
(4)反应②的离子方程式为 .
查看习题详情和答案>>

依据上述信息,回答下列的问题:
(1)J在元素周期表中的位置是
(2)F的水溶液显
(3)反应①的化学方程式为
(4)反应②的离子方程式为
物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G 的浓溶液中发生钝化, F 的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。

请讨论以下两种情况(注:两种情况下各字母代表的物质可能不同) 回答下列问题:
(1)第一种情况:用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
①反应Ⅲ的化学方程式为_____________________。
②D与乙反应的离子方程式为_____________________。
(2)第二种情况: 甲由两种单质直接化合得到;B 为红棕色固体; C为无色气体,是形成酸雨的大气污染物之一;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
①工业上,反应 I的化学方程式为______________________________________。
②D和乙反应的离子方程式为____________________________________ 。
③ 请简述检验D溶液中阳离子的方法___________ 。
④ 若A的相对分子质量为120,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=_____________(列出计算式即可)。
查看习题详情和答案>>
(1)第一种情况:用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
①反应Ⅲ的化学方程式为_____________________。
②D与乙反应的离子方程式为_____________________。
(2)第二种情况: 甲由两种单质直接化合得到;B 为红棕色固体; C为无色气体,是形成酸雨的大气污染物之一;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
①工业上,反应 I的化学方程式为______________________________________。
②D和乙反应的离子方程式为____________________________________ 。
③ 请简述检验D溶液中阳离子的方法___________ 。
④ 若A的相对分子质量为120,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=_____________(列出计算式即可)。
物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G的浓溶液中发生钝化,F的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明).请讨论以下两种情况(注:两种情况下各字母代表的物质可能不同)
回答下列问题:
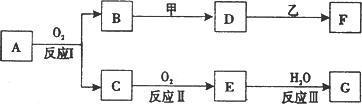
(1)第一种情况:用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质;D和F的溶液均呈碱性.则:
①反应Ⅲ的化学方程式为________.
②D与乙反应的离子方程式为________
(2)第二种情况:甲由两种单质直接化合得到;B为红棕色固体;C为无色气体,是形成酸雨的大气污染物之一;D的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成.则:
①工业上,反应I的化学方程式为________
生产设备名称为:________
②D和乙反应的离子方程式为________
③请简述检验D溶液中阳离子的方法________.
④若A的相对分子质量为120,反应Ⅰ、Ⅱ、Ⅲ均为完全转化.现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρ g/cm3,溶质质量分数为a%的G溶液n mL.则该样品中A的质量分数=________(列出计算式即可).
有①~⑩十种元素,原子序数依次增大,⑨、⑩为第四周期过渡元素,其余均为短周期元素.

(1)若②、⑦、⑧三种元素在周期表中相对位置如下:
由②形成的化合物种类最多,则②、⑦、⑧三种元素最高价氧化物的水化物酸性由强到弱的顺序是
(2)甲、乙、丙、丁、戊均为上述短周期元素中的某些单质或由其中两种元素组成的化合物,且甲、戊为无色气体,反应a为置换反应,反应b为化合反应.见右图示转化关系推测:戊可能为
(3)若图1中A、B、C、D、E分别是上述10种元素中的某些单质或其中两种元素组成的化合物.已知:A是常见金属,D、E分别为无色和黄绿色气体,反应c是用A作电极,在B的水溶液中进行的电解反应,属于置换反应类型.它们的转化关系如图2示.则反应d中阴极的电极反应式为
若反应c是在高温下进行的,且为工业上有重要应用价值的放热反应,物质C是一种两性化合物,则反应c的化学方程式
查看习题详情和答案>>

(1)若②、⑦、⑧三种元素在周期表中相对位置如下:
| ② | |||
| ⑦ | ⑧ |
HClO4>H2SO4>H2CO3
HClO4>H2SO4>H2CO3
(用化学式表示).(2)甲、乙、丙、丁、戊均为上述短周期元素中的某些单质或由其中两种元素组成的化合物,且甲、戊为无色气体,反应a为置换反应,反应b为化合反应.见右图示转化关系推测:戊可能为
CO、SO2、NO
CO、SO2、NO
(列举一例).(3)若图1中A、B、C、D、E分别是上述10种元素中的某些单质或其中两种元素组成的化合物.已知:A是常见金属,D、E分别为无色和黄绿色气体,反应c是用A作电极,在B的水溶液中进行的电解反应,属于置换反应类型.它们的转化关系如图2示.则反应d中阴极的电极反应式为
Cu2++2e-═Cu
Cu2++2e-═Cu
.若反应c是在高温下进行的,且为工业上有重要应用价值的放热反应,物质C是一种两性化合物,则反应c的化学方程式
Fe2O3+2Al
2Fe+Al2O3
| ||
Fe2O3+2Al
2Fe+Al2O3
.
| ||
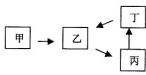 甲、乙、丙、丁四种物质有如图所示的转化关系,已知甲是地壳中含量最高的元素组成的单质,常见化合物乙、丙、丁均含有短周期一种相同元素(除组成甲的元素外).
甲、乙、丙、丁四种物质有如图所示的转化关系,已知甲是地壳中含量最高的元素组成的单质,常见化合物乙、丙、丁均含有短周期一种相同元素(除组成甲的元素外).(1)若丁的稀溶液与铜反应可生成乙,写出反应的离子方程式:
(2)若乙是难溶于水的酸性氧化物,写出工业上以乙为原料制取所含元素单质的化学方程式:
(3)若丙是离子化合物,且阴离子含有金属元素M.
①写出过量的二氧化碳通入丙溶液制取丁的离子方程式:
②以色列科学家Daniel Shechtman因发现准晶体获得2011年诺贝尔化学奖.人们在自然界中也找到了组成为M63Cu24Fe13的天然准晶体.将相同质量的此准品体分别与足量的盐酸、烧碱和稀硝酸反应,产生气体的物质的量关系为
A.n(烧碱)<n(稀硝酸)<n(盐酸) B.n(烧碱)<n(盐酸)<n(稀硝酸)
C.n(稀硝酸)<n(烧碱)<n(盐酸) D.n(盐酸)<n(稀硝酸)<n(烧碱)
(4)若乙含有第三周期元素A,2乙(g)+甲(g)?2丙(g)是工业生产中重要反应之一.
①写出实现NalO3+NaHAO3→I2+Na2AO4+H2AO4转化的配平并标明电子转移的方向和数目的化学方程式:
②已知:还原性HAO3->I-,若加入的NaHAO3过量,还可能与上述生成物中的