摘要:本章教学内容包含三节:物质的分类.离子反应.氧化还原反应.1.物质的分类一节.要求的深广度为:①知道物质的分类在学习科学和日常生活中的意义.②学会不同分类标准进行分类.③分散系的种类.胶体的定义及其与溶液的区别.不宜扩展的是科学视野中的内容.对于胶体知识点.我们只要求知道胶体概念及其与其它分散系的区别.
网址:http://m.1010jiajiao.com/timu_id_3998365[举报]
本章可认为是对初中所学化学反应的系统分类,是站在不同角度来分类的.下列对各种分类依据的叙述正确的是
①依据反应物和生成物的类别以及反应前后物质的种类的多少,把化学反应分为化合反应、分解反应、置换反应、复分解反应
②依据反应中是否有电子转移(得失或偏移),把化学反应分为氧化还原反应和非氧化还原反应
③依据电解质在溶液里所起反应的实质,把化学反应分为离子反应和非离子反应
④依据化学反应中的能量变化(通常表现为热量的变化),把化学反应分为放热反应和吸热反应
- A.只有①②③正确
- B.都不正确
- C.都正确
- D.只有②③④正确
|
本章可认为是对初中所学化学反应的系统分类,是站在不同角度来分类的.下列对各种分类依据的叙述正确的是 ①依据反应物和生成物的类别以及反应前后物质的种类的多少,把化学反应分为化合反应、分解反应、置换反应、复分解反应 ②依据反应中是否有电子转移(得失或偏移),把化学反应分为氧化还原反应和非氧化还原反应 ③依据电解质在溶液里所起反应的实质,把化学反应分为离子反应和非离子反应 ④依据化学反应中的能量变化(通常表现为热量的变化),把化学反应分为放热反应和吸热反应 | |
| [ ] | |
A. |
只有①②③正确 |
B. |
都不正确 |
C. |
都正确 |
D. |
只有②③④正确 |
硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容.
(1)对比研究是一种重要的研究方法.若将硫的单质及部分化合物按如下表所示分成3组,则第2组中物质M的化学式是 .
(2)某校化学学习小组用下图所示的实验装置研究SO2的性质.

①在装置Ⅰ中发生SO2的催化氧化反应,其化学方程式是 .
②若按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,(已知:SO3熔点 16.8℃; SO2 沸点-10℃.)装置Ⅱ的作用是 ;装置Ⅲ中溶液逐渐褪色,生成Mn2+的同时pH降低,则该反应的离子方程式是 .
③若按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,如果装置Ⅳ中有30mL 2.5mol/LNaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的化学方程式是 .
查看习题详情和答案>>
(1)对比研究是一种重要的研究方法.若将硫的单质及部分化合物按如下表所示分成3组,则第2组中物质M的化学式是
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |

①在装置Ⅰ中发生SO2的催化氧化反应,其化学方程式是
②若按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,(已知:SO3熔点 16.8℃; SO2 沸点-10℃.)装置Ⅱ的作用是
③若按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,如果装置Ⅳ中有30mL 2.5mol/LNaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的化学方程式是
 (2010?烟台一模)2008年5月12日我国四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒液,如NaClO溶液.某校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究.
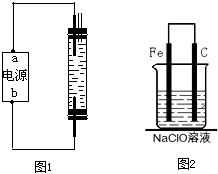
(2010?烟台一模)2008年5月12日我国四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒液,如NaClO溶液.某校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究.甲同学:为制备消毒液,探究并制作了一种家用环保型消毒液(NaClO溶液)发生器,设计了如图1所示的装置,用石墨作电极电解饱和氯化钠溶液.
请完成下列问题:若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源的a电极名称为
负
负
极(填“正”、“负”、“阴”或“阳”),与其相连的电极的电极反应式为2H++2e-→H2↑
2H++2e-→H2↑
;装置溶液中反应生成NaClO的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O
Cl2+2OH-═Cl-+ClO-+H2O
.乙同学:从某超市中查询到某品牌消毒液包装说明的部分内容摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L.可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用.切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品.本品须密封,置阴凉暗处保存.
请完成以下实验探究过程:
Ⅰ.阅读材料,根据学过的知识判断问题
(1)室温条件下,该消毒液(NaClO)溶液的pH
>
>
7(填“>”、“<”或“=”),原因是(用离子方程式表示)
ClO-+H2O?HClO+OH-
ClO-+H2O?HClO+OH-
.(2)该消毒液还具有的化学性质是
A、D
A、D
(填序号).A.强氧化性 B.强还原性 C.不稳定性 D.漂白性 E.弱酸性
Ⅱ.确定要研究的问题
该消毒液对碳钢制品的腐蚀原理.
Ⅲ.设计方案,实施探究
(1)用烧杯取少量样品,将一颗光亮的普通碳钢钉放入烧杯,浸泡一段时间.预期的实验现象是
钢钉表面有红褐色物质生成
钢钉表面有红褐色物质生成
.(2)为了进一步探究碳钢钉在该消毒液(NaClO)中的腐蚀原理,丁同学设计了如图2实验装置,写出碳(C)极上发生的电极反应式
ClO-+2e-+H2O→Cl-+2OH-
ClO-+2e-+H2O→Cl-+2OH-
. 下面是关于药物华素片(西地碘片)使用说明书中的部分内容.
下面是关于药物华素片(西地碘片)使用说明书中的部分内容.华素片(西地碘片)说明书[药品名称]通用名:西地碘片商品名:华素片[药物组成]本品主要活性成分是分子碘,含量1.5mg/片.将碘利用分子分散技术制成分子态西地碘,辅料为蔗糖等.
(1)根据上述说明和所学化学知识回答:
①华素片中含有的活性成分是
I2
I2
(写分子式).②华素片的贮藏方法
避光、密闭、阴凉处
避光、密闭、阴凉处
.(2)某学生为验证华素片中确实含有上述活性成分,完成实验如下,请填写:
①取一粒药片放入研钵中研碎,再将药粉装入试管并加入约2mL蒸馏水;向该试管中再加入约2mL
C
C
(填选项字母),并用力振荡;A.酒精 B.NaOH溶液 C.四氯化碳 D.盐酸
②描述加入该液体后观察到的现象
溶液分层,下层紫红色
溶液分层,下层紫红色
;③选用该液体做实验的原因是
CCl4与水互不相溶,且碘在CCl4中的溶解度比在水中溶解度大
CCl4与水互不相溶,且碘在CCl4中的溶解度比在水中溶解度大
.(3)请再设计另一种方法,验证华素片中的活性成分(简述实验操作、现象和结论).
取一粒华素片研细,先溶于水配成溶液,再滴加淀粉溶液,如溶液变蓝,说明华素片含碘
取一粒华素片研细,先溶于水配成溶液,再滴加淀粉溶液,如溶液变蓝,说明华素片含碘
.