摘要:电极判断,负极:(1) 金属 ,(2)电子流 的极, (3)发生 反应的电极.正极(1) 金属 ,(2)电子流 的极, (3)发生 反应的电极.注意:(!) 原电池构成的本质条件:某一电极要能与电解质溶液的中某种成分反应. (2)很活泼的金属单质不可做原电池的负极,如K.Na.Ca等(3)在原电池的电解质溶液内,阳离子移向正极,阴离子移向负极.(4)两极得失电子数相等 二. 燃料电池 它以还原剂(甲醇.氢气.一氧化碳.甲烷等作燃料)为负极反应物,以氧化剂 为正极反应物.电解质则有碱性.酸性.熔融盐和固体电解质.[例题解析]
网址:http://m.1010jiajiao.com/timu_id_399761[举报]
把A、B、C、D四块金属浸入稀硫酸溶液中,用导线两两相连组成原电池.若A、B相连时,A为负极;C、D相连时,D极产生大量气泡; A、C相连时,C极发生还原反应;B、D相连时,电子由D经导线流向B.据此,判断四种金属的活动性顺序由强到弱是( )
查看习题详情和答案>>
把A、B、C、D四块金属浸入稀硫酸溶液中,用导线两两相连组成原电池.若A、B相连时,A为负极;C、D相连时,D极产生大量气泡; A、C相连时,C极发生还原反应;B、D相连时,电子由D经导线流向B.据此,判断四种金属的活动性顺序由强到弱是( )
A.A>B>C>D
B.A>C>D>B
C.C>A>B>D
D.B>D>C>A
查看习题详情和答案>>
A.A>B>C>D
B.A>C>D>B
C.C>A>B>D
D.B>D>C>A
查看习题详情和答案>>
原电池的正负极的判断:
①由组成原电池的两极材料判断。一般是 的金属为负极,活泼性 的金属或能 的非金属为正极。
②根据电流方向或电子流动方向判断。电流是由 流向 ;电子流动方向是由 极流向 极。
③根据原电池里电解质溶液内离子的定向流动方向。在原电池的电解质溶液内,阳离子移向的极是 极,阴离子移向的极为 极。
④根据原电池两极发生的变化来判断。原电池的负极总是 电子发生氧化反应,其正极总是 电子发生 反应。
查看习题详情和答案>>(1)1780年,意大利解剖学家伽伐尼在用银质手术刀触碰放在铁盘上的青蛙的时候,无意间发现青蛙腿部肌肉抽搐了一下,仿佛受到电流的刺激.如果只用一种金属器械去触动青蛙,就无此种反应.伽伐尼认为出现这种现象的原因是动物体内存在“生物电”.结合你所学的知识模拟该过程,下列哪种材质的手术刀触碰铁盘上的青蛙腿不会产生触动?
a 铝 b 陶瓷 c 塑料 d 铁
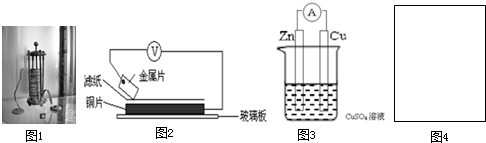
(2)1799年,伏打仔细研究了伽伐尼的发现,以含食盐水的湿抹布,夹在银和锌的圆形版中间,堆积成圆柱状,制造出世界上最早的电池-伏打电池(图1). 将洁净的金属片A、B、D、E分别放置在浸有盐溶液的滤纸上面并压紧(如图2所示).在每次实验时,记录电压表指针的移动方向和电压表的读数如下:
已知:构成两电极的金属其金属活泼性相差越大,电压表的读数越大.请依据表中数据判断:
(3)1836年,英国科学家丹尼尔对伏打电池进行改进,获得了世界上第一个能够获得稳定电流的电池,图3是丹尼尔电池的简易装置:
该电池的正极是
(4)随着社会的发展和科技的进步,越来越多的电池被制造出来.请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+以“ ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
查看习题详情和答案>>
bcd
bcd
(填字母)a 铝 b 陶瓷 c 塑料 d 铁

(2)1799年,伏打仔细研究了伽伐尼的发现,以含食盐水的湿抹布,夹在银和锌的圆形版中间,堆积成圆柱状,制造出世界上最早的电池-伏打电池(图1). 将洁净的金属片A、B、D、E分别放置在浸有盐溶液的滤纸上面并压紧(如图2所示).在每次实验时,记录电压表指针的移动方向和电压表的读数如下:
| 金属 | 电子流动方向 | 电压(V) |
| A | A→Cu | +0.78 |
| B | Cu→B | -0.15 |
| D | D→Cu | +1.35 |
| E | E→Cu | +0.30 |
D
D
金属可能是最强的还原剂;B
B
金属一定不能从硫酸铜溶液中置换出铜.(3)1836年,英国科学家丹尼尔对伏打电池进行改进,获得了世界上第一个能够获得稳定电流的电池,图3是丹尼尔电池的简易装置:
该电池的正极是
铜
铜
,负极是锌
锌
,正极反应是Cu2++2e-=Cu
Cu2++2e-=Cu
,负极反应是Zn-2e-=Fe2+
Zn-2e-=Fe2+
.(4)随着社会的发展和科技的进步,越来越多的电池被制造出来.请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+以“
 ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.