摘要:了解合成氨工业的反应原理和生产阶段.主要设备,
网址:http://m.1010jiajiao.com/timu_id_399361[举报]
合成氨工业及硝酸工业对工、农生产和国防都有重要意义。请回答:
(1)以N2和H2为原料合成氨气。已知:N2(g)+3H2(g) 2NH3(g);△H= -92.4 kJ/mol,
2NH3(g);△H= -92.4 kJ/mol,
①合成氨工业中采取的下列措施可以用勒夏特列原理解释的是(填选项序号)_______。
a.用铁触媒加快化学反应速率
b.采用较高压强(20 MPa~50 MPa)
c.将原料气中的少量CO等气体净化除去
d.将生成的氨液化并及时从体系中分离出来
②一定温度下,在密闭容器中充入1 mol N2和3 mol H2并发生反应。
a.若容器容积恒定,达到平衡时气体的压强为原来的7/8,N2的转化率为а1,此时,反应放热为_________kJ;
b.若容积为4L,当进行到第4分钟时达到平衡,生成NH3为1.0 mol,则从开始到达平衡时NH3的平均速率v(NH3)=_________。
c.若容器压强恒定,则达到平衡时,容器中N2的转化率为а2,则а2_______а1(填“>、<或=”)。
(2)以氨气、空气为主要原料制硝酸。
①NH3被氧气催化氧化生成NO的反应的化学方程式是______________________。
②硝酸厂常用如下2种方法处理尾气。
a.催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是___________________。
b.碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。若每9.2gNO2和Na2CO3溶液反应时转移电子数为0.1mol,则反应的离子方程式是_______________。
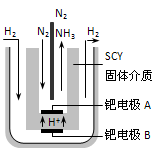
(3)随着对合成氨研究的发展,希腊科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。钯电极A是电解池的_______极(填“阳”或“阴”),该极上的电极反应式是__________________ 。
(1)以N2和H2为原料合成氨气。已知:N2(g)+3H2(g)
 2NH3(g);△H= -92.4 kJ/mol,
2NH3(g);△H= -92.4 kJ/mol,①合成氨工业中采取的下列措施可以用勒夏特列原理解释的是(填选项序号)_______。
a.用铁触媒加快化学反应速率
b.采用较高压强(20 MPa~50 MPa)
c.将原料气中的少量CO等气体净化除去
d.将生成的氨液化并及时从体系中分离出来
②一定温度下,在密闭容器中充入1 mol N2和3 mol H2并发生反应。
a.若容器容积恒定,达到平衡时气体的压强为原来的7/8,N2的转化率为а1,此时,反应放热为_________kJ;
b.若容积为4L,当进行到第4分钟时达到平衡,生成NH3为1.0 mol,则从开始到达平衡时NH3的平均速率v(NH3)=_________。
c.若容器压强恒定,则达到平衡时,容器中N2的转化率为а2,则а2_______а1(填“>、<或=”)。
(2)以氨气、空气为主要原料制硝酸。
①NH3被氧气催化氧化生成NO的反应的化学方程式是______________________。
②硝酸厂常用如下2种方法处理尾气。
a.催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是___________________。
b.碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。若每9.2gNO2和Na2CO3溶液反应时转移电子数为0.1mol,则反应的离子方程式是_______________。
(3)随着对合成氨研究的发展,希腊科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。钯电极A是电解池的_______极(填“阳”或“阴”),该极上的电极反应式是__________________ 。
工业制硫酸的尾气中含有一定量SO2,处理尾气的手段除了氨吸收法以外还有以下几种方法.
(一)工业实际吸收过程中,第I步常采用浓苛性钠溶液吸收为其中的SO2,然后向生成溶液中加入熟石灰,充分反应后将生成产物分离后再经氧化后制得产品A.

(1)产品A是
(2)有人提出将第一步中的浓苛性钠溶液换成同温度下饱和Ca(OH)2溶液直接制得产品CaSO3,你认为是否可行?
(二)制备MnSO4?H2O:SO2还原MnO2矿制备MnSO4?H2O,过程如下:

(1)生产中提高MnO2矿浸出率的措施除了将矿石粉碎还有
(2)除铁发生的离子反应方程式为
(3)操作I的名称为
(4)MnSO4?H2O在1150℃高温下易分解,产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是
查看习题详情和答案>>
(一)工业实际吸收过程中,第I步常采用浓苛性钠溶液吸收为其中的SO2,然后向生成溶液中加入熟石灰,充分反应后将生成产物分离后再经氧化后制得产品A.

(1)产品A是
CaSO4
CaSO4
(填化学式).(2)有人提出将第一步中的浓苛性钠溶液换成同温度下饱和Ca(OH)2溶液直接制得产品CaSO3,你认为是否可行?
不可以
不可以
(填“可以”、“不可以”或“不确定”)原因是Ca(OH)2在水中溶解度较小,c(OH-)太低,吸收效率不高
Ca(OH)2在水中溶解度较小,c(OH-)太低,吸收效率不高
(二)制备MnSO4?H2O:SO2还原MnO2矿制备MnSO4?H2O,过程如下:

(1)生产中提高MnO2矿浸出率的措施除了将矿石粉碎还有
充分搅拌、适当提高体系温度等
充分搅拌、适当提高体系温度等
(答出一条即可).(2)除铁发生的离子反应方程式为
2Fe3++3H2O+3CaCO3=2Fe(OH)3↓+3CO2↑+3Ca2+ 或Fe3++3H2O  Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O
Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O
 Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O
Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O2Fe3++3H2O+3CaCO3=2Fe(OH)3↓+3CO2↑+3Ca2+ 或Fe3++3H2O  Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O
Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O
. Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O
Fe(OH)3+3H+ 2H++CaCO3=Ca2++CO2↑+H2O(3)操作I的名称为
蒸发浓缩、冷却结晶
蒸发浓缩、冷却结晶
.(4)MnSO4?H2O在1150℃高温下易分解,产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是
3MnSO4?H2O Mn3O4+SO2↑+2SO3↑+3H2O
Mn3O4+SO2↑+2SO3↑+3H2O
 Mn3O4+SO2↑+2SO3↑+3H2O
Mn3O4+SO2↑+2SO3↑+3H2O3MnSO4?H2O Mn3O4+SO2↑+2SO3↑+3H2O
Mn3O4+SO2↑+2SO3↑+3H2O
. Mn3O4+SO2↑+2SO3↑+3H2O
Mn3O4+SO2↑+2SO3↑+3H2O工业制硫酸的尾气中含有一定量SO2,处理尾气的手段除了氨吸收法以外还有以下几种方法.
(一)工业实际吸收过程中,第I步常采用浓苛性钠溶液吸收为其中的SO2,然后向生成溶液中加入熟石灰,充分反应后将生成产物分离后再经氧化后制得产品A.

(1)产品A是______(填化学式).
(2)有人提出将第一步中的浓苛性钠溶液换成同温度下饱和Ca(OH)2溶液直接制得产品CaSO3,你认为是否可行?______(填“可以”、“不可以”或“不确定”)原因是______
(二)制备MnSO4?H2O:SO2还原MnO2矿制备MnSO4?H2O,过程如下:

(1)生产中提高MnO2矿浸出率的措施除了将矿石粉碎还有______(答出一条即可).
(2)除铁发生的离子反应方程式为______.
(3)操作I的名称为______.
(4)MnSO4?H2O在1150℃高温下易分解,产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是______.
查看习题详情和答案>>
工业制硫酸的尾气中含有一定量SO2,处理尾气的手段除了氨吸收法以外还有以下几种方法.
(一)工业实际吸收过程中,第I步常采用浓苛性钠溶液吸收为其中的SO2,然后向生成溶液中加入熟石灰,充分反应后将生成产物分离后再经氧化后制得产品A.

(1)产品A是______(填化学式).
(2)有人提出将第一步中的浓苛性钠溶液换成同温度下饱和Ca(OH)2溶液直接制得产品CaSO3,你认为是否可行?______(填“可以”、“不可以”或“不确定”)原因是______
(二)制备MnSO4?H2O:SO2还原MnO2矿制备MnSO4?H2O,过程如下:

(1)生产中提高MnO2矿浸出率的措施除了将矿石粉碎还有______(答出一条即可).
(2)除铁发生的离子反应方程式为______.
(3)操作I的名称为______.
(4)MnSO4?H2O在1150℃高温下易分解,产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是______.
查看习题详情和答案>>
(一)工业实际吸收过程中,第I步常采用浓苛性钠溶液吸收为其中的SO2,然后向生成溶液中加入熟石灰,充分反应后将生成产物分离后再经氧化后制得产品A.

(1)产品A是______(填化学式).
(2)有人提出将第一步中的浓苛性钠溶液换成同温度下饱和Ca(OH)2溶液直接制得产品CaSO3,你认为是否可行?______(填“可以”、“不可以”或“不确定”)原因是______
(二)制备MnSO4?H2O:SO2还原MnO2矿制备MnSO4?H2O,过程如下:

(1)生产中提高MnO2矿浸出率的措施除了将矿石粉碎还有______(答出一条即可).
(2)除铁发生的离子反应方程式为______.
(3)操作I的名称为______.
(4)MnSO4?H2O在1150℃高温下易分解,产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是______.
查看习题详情和答案>>
合成氨工业对国民经济和社会发展具有重要的意义.其原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
据此回答以下问题:
(1)从化学平衡角度考虑,为了提高氨气的产率,可以选择的方法是
①升高温度 ②增大压强 ③使用催化剂 ④及时分离出NH3
(2)对在恒容密闭容器中进行的可逆反应:N2(g)+3H2(g)?2NH3(g),下列选项中说明该反应已经达到化学平衡状态是:
①N2的消耗应速率是NH3的消耗速率的1/2
②在恒容条件下,混合气体的压强保持不变
③N2、H2、NH3的物质的量之比为1:3:2
④单位时间内每生成3mol H2的同时有2mol NH3生成
⑤3mol N-N键断裂,同时有6mol N-H键断裂
(3)一定条件下,NH3在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是
查看习题详情和答案>>
据此回答以下问题:
(1)从化学平衡角度考虑,为了提高氨气的产率,可以选择的方法是
②④
②④
(填序号,错选扣分).①升高温度 ②增大压强 ③使用催化剂 ④及时分离出NH3
(2)对在恒容密闭容器中进行的可逆反应:N2(g)+3H2(g)?2NH3(g),下列选项中说明该反应已经达到化学平衡状态是:
①②④
①②④
.(填序号).①N2的消耗应速率是NH3的消耗速率的1/2
②在恒容条件下,混合气体的压强保持不变
③N2、H2、NH3的物质的量之比为1:3:2
④单位时间内每生成3mol H2的同时有2mol NH3生成
⑤3mol N-N键断裂,同时有6mol N-H键断裂
(3)一定条件下,NH3在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是
ac
ac
(选填序号).| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入NH3的物质的量 |
| y | NH3的物质的量 | 平衡常数K | NH3的转化率 | 生成物物质的量总和 |