摘要:在一体积为1L的密闭容器中发生反应:2HI(g) H2(g) + I2(g) .当HI气体的起始浓度为1mol/L.H2和I2气体的起始浓度为0时.出现如下可能的图像 下列有关说法正确的是( ) A.甲.乙中的反应温度不同.压强相同 B.甲中可能未使用催化剂.乙中可能使用了催化剂 C.丙中的平衡混合物中.物质H2的浓度等于0.6mol/L D.丁和乙比较.丁中可能增大了反应体系的压强 [答案]选B.
网址:http://m.1010jiajiao.com/timu_id_3991755[举报]
(2010?海南)I已知: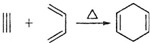 ,如果要合成
,如果要合成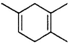 所用的原始原料可以是
所用的原始原料可以是
A.2-甲基-l,3-丁二烯和2-丁炔 B.1,3-戊二烯和2-丁炔
C.2,3-二甲基-1,3-戊二烯和乙炔 D.,3-二甲基-l,3-丁二烯和丙炔
II(A~G都是有机化合物,它们的转化关系如下: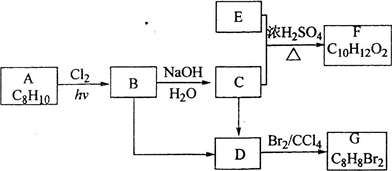
请回答下列问题:
(1)已知:6.0g化合物E完全燃烧生成8.8g C02和3.6g H20;E的蒸气与氢气的相对密度为30,则E的分子式为
(2)A为一取代芳烃,B中含有一个甲基.由B生成C的化学方程式为
(3)由B生成D、由C生成D的反应条件分别是
(4)由A生成B、由D生成G的反应类型分别是
(5)F存在于栀子香油中,其结构简式为
 ;
;
(6)在G的同分异构体中,苯环上一硝化的产物只有一种的共有
 (填结构简式).
(填结构简式).
查看习题详情和答案>>
 ,如果要合成
,如果要合成 所用的原始原料可以是
所用的原始原料可以是AD
AD
A.2-甲基-l,3-丁二烯和2-丁炔 B.1,3-戊二烯和2-丁炔
C.2,3-二甲基-1,3-戊二烯和乙炔 D.,3-二甲基-l,3-丁二烯和丙炔
II(A~G都是有机化合物,它们的转化关系如下:

请回答下列问题:
(1)已知:6.0g化合物E完全燃烧生成8.8g C02和3.6g H20;E的蒸气与氢气的相对密度为30,则E的分子式为
C2H4O2
C2H4O2
:(2)A为一取代芳烃,B中含有一个甲基.由B生成C的化学方程式为
C6H5CHClCH3+H2O
C6H5CHOHCH3+HCl
| NaOH |
| △ |
C6H5CHClCH3+H2O
C6H5CHOHCH3+HCl
;| NaOH |
| △ |
(3)由B生成D、由C生成D的反应条件分别是
NaOH醇溶液并加热
NaOH醇溶液并加热
、浓硫酸并加热
浓硫酸并加热
;(4)由A生成B、由D生成G的反应类型分别是
取代反应
取代反应
、加成反应
加成反应
;(5)F存在于栀子香油中,其结构简式为


(6)在G的同分异构体中,苯环上一硝化的产物只有一种的共有
7
7
个,其中核磁共振氢谱有两组峰,且峰面积比为l:1的是

(2010?海南)根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量Ar(Cu)(近似值)的实验.先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算Ar(Cu).为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→
(3)在本实验中,若测得m(CuO)=a g,m(H2O)=b g,则Ar(Cu)=
-16
-16;
(4)在本实验中,使测定结果Ar(Cu)偏大的是
①Cu0未完全起反应 ②CuO不干燥 ③Cu0中混有不反应的杂质 ④碱石灰不干燥 ⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定
查看习题详情和答案>>

请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为
2NH3+3CuO
3Cu+3H2O+N2
| ||
2NH3+3CuO
3Cu+3H2O+N2
;
| ||
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→
e→b→e
e→b→e
;(3)在本实验中,若测得m(CuO)=a g,m(H2O)=b g,则Ar(Cu)=
| 18a |
| b |
| 18a |
| b |
(4)在本实验中,使测定结果Ar(Cu)偏大的是
①③
①③
(填序号);①Cu0未完全起反应 ②CuO不干燥 ③Cu0中混有不反应的杂质 ④碱石灰不干燥 ⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定
m(CuO)
m(CuO)
和m(Cu)
m(Cu)
,或m(Cu)
m(Cu)
和m(H2O)
m(H2O)
达到实验目的.