摘要:14.有关FeCI3溶液和氢氧化铁胶体分析错误的是 A.加入NaOH溶液均可出现棕色沉淀, B.加热蒸干且灼烧固体均可得氧化铁, C.若过滤时.分散质均能能透过滤纸, D.可见光光照时二者分散系均可看到光路通过,
网址:http://m.1010jiajiao.com/timu_id_3990762[举报]
格隆溴铵具有解痉、减少胃酸分泌等作用,用于治疗胃及十二指肠溃疡,合成路线如下:

(1)化合物I的分子式为 。
(2)反应①的化学方程式为 ;反应②的反应类型是加成反应,该反应的另一种反应物的结构简式是 。
(3)化合物IV的结构简式为 。
(4)有关对化合物III、IV、V的说法,正确的是 。
a.能燃烧,产物均是CO2和H2O b.均能与NaOH溶液反应
c.均能发生消去反应 d.均能使溴水因反应而褪色
(5)化合物I有多种同分异构体,其中能发生与FeCI3溶液的显色反应和银镜反应,且苯环 上有两种化学环境不同的氢原子的结构简式为 (任写一种)。
查看习题详情和答案>>
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下,请回答下列问题: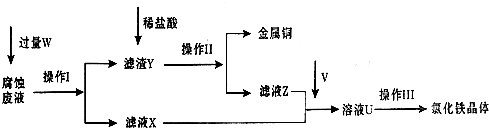
(1)请写出FeCl3溶液与铜反应的离子方程式:
(2)操作Ⅱ之前最好加入适量稀盐酸,某同学用10mol?L-1 的浓盐酸配制250mL 1mol?L-1 的稀盐酸,并进行有关实验.
①需要量取浓盐酸
②配制该稀盐酸时除量筒、烧杯、玻璃棒外,还必须用到的仪器有
③用已知浓度的氢氧化钠溶液滴定稀盐酸,滴定过程中眼睛应注视
(3)操作Ⅲ前需要通入气体V,请写出实验室制取气体V的化学方程式:
(4)操作Ⅲ应在HCl气流氛围中进行,其原因是
(5)若通入的V的量不足,则最后制得的氯化铁晶体不纯净,这是因为溶液U中含有杂质
供选择的试剂:酸性KMnO4溶液、KSCN溶液、氯水.
(6)若向氯化铁溶液中加入一定量石灰水,调节溶液pH,可得红褐色沉淀.该过程中调节溶液的pH为5,则金属离子浓度为
查看习题详情和答案>>

(1)请写出FeCl3溶液与铜反应的离子方程式:
2Fe3++Cu═2Fe2++Cu2+
2Fe3++Cu═2Fe2++Cu2+
;操作Ⅰ加入的试剂W是铁粉或Fe
铁粉或Fe
.(2)操作Ⅱ之前最好加入适量稀盐酸,某同学用10mol?L-1 的浓盐酸配制250mL 1mol?L-1 的稀盐酸,并进行有关实验.
①需要量取浓盐酸
25mL
25mL
mL.②配制该稀盐酸时除量筒、烧杯、玻璃棒外,还必须用到的仪器有
250mL容量瓶
250mL容量瓶
、胶头滴管
胶头滴管
.③用已知浓度的氢氧化钠溶液滴定稀盐酸,滴定过程中眼睛应注视
锥形瓶内溶液颜色的变化
锥形瓶内溶液颜色的变化
,实验时未用标准液润洗滴定管,测得锥形瓶中待测液的浓度大于
大于
实际浓度.(填“>”、“<”或“=”).(3)操作Ⅲ前需要通入气体V,请写出实验室制取气体V的化学方程式:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
,该反应中
| ||
MnO2
MnO2
是氧化剂.(4)操作Ⅲ应在HCl气流氛围中进行,其原因是
抑制Fe3+(或FeCI3)的水解
抑制Fe3+(或FeCI3)的水解
.(5)若通入的V的量不足,则最后制得的氯化铁晶体不纯净,这是因为溶液U中含有杂质
FeCl2或Fe2+
FeCl2或Fe2+
.请设计合理的实验,验证溶液U中的成分,并判断通入的V的量是否不足取少量溶液U,加入几滴KSCN溶液,溶液显红色,则表明溶液U中有Fe3+(FeCl3);另取少量溶液U,加入几滴酸性KMnO4溶液,若KMnO4溶液退色,则表明溶液U中有Fe2+(或FeCl2),说明通入的V的量不足够若KMnO4溶液不退色,则说明通入的V的量充足
取少量溶液U,加入几滴KSCN溶液,溶液显红色,则表明溶液U中有Fe3+(FeCl3);另取少量溶液U,加入几滴酸性KMnO4溶液,若KMnO4溶液退色,则表明溶液U中有Fe2+(或FeCl2),说明通入的V的量不足够若KMnO4溶液不退色,则说明通入的V的量充足
(简要说明实验步骤、现象和结论).供选择的试剂:酸性KMnO4溶液、KSCN溶液、氯水.
(6)若向氯化铁溶液中加入一定量石灰水,调节溶液pH,可得红褐色沉淀.该过程中调节溶液的pH为5,则金属离子浓度为
4.0×10-11mol?L-1
4.0×10-11mol?L-1
.(己知:Ksp[Fe(OH)3]=4.0×10-38)