摘要:极性分子:(1)含义: .(2)举例: .
网址:http://m.1010jiajiao.com/timu_id_398888[举报]
(2013?普陀区二模)用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,反应如下:3SiCl4+2N2+6H2
Si3N4+12HCl
完成下列填空:
(1)氮化硅可用于制造发动机的耐热部件,因为它属于
 .
.
(2)比较Si和Cl两种元素非金属性强弱的方法是
a.比较两种元素的气态氢化物的沸点
b.比较两种元素的原子获得一个电子时释放能量的大小
c.比较两种元素的原子达到稳定结构获得电子的多少
d.比较相同条件下两种元素氢化物水溶液的酸性强弱
(3)Si与Al、Be具有相似的化学性质,因为
查看习题详情和答案>>
| 高温 |
完成下列填空:
(1)氮化硅可用于制造发动机的耐热部件,因为它属于
原子
原子
晶体.有关氮化硅的上述反应中,原子最外层只有一个未成对电子的元素是H、Cl
H、Cl
(填写元素符号);属于非极性分子的化合物的电子式是

(2)比较Si和Cl两种元素非金属性强弱的方法是
b
b
.a.比较两种元素的气态氢化物的沸点
b.比较两种元素的原子获得一个电子时释放能量的大小
c.比较两种元素的原子达到稳定结构获得电子的多少
d.比较相同条件下两种元素氢化物水溶液的酸性强弱
(3)Si与Al、Be具有相似的化学性质,因为
它们都在元素周期表中金属和非金属的分界线附近
它们都在元素周期表中金属和非金属的分界线附近
(简述理由),写出Si与强碱溶液反应的离子反应方程式:Si+2OH-+H2O=SiO32-+2H2↑
Si+2OH-+H2O=SiO32-+2H2↑
.I.有下列物质:①冰醋酸 ②金刚石 ③碳化硅 ④干冰 ⑤过氧化氢 ⑥白磷
根据要求用序号填空.
(1)属于原子晶体的化合物是
II.在①H2O、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2、⑧C2H2分子中:
(1)全部以非极性键结合的非极性分子是
(2)全部以极性键相结合,具有直线型结构的非极性分子是
(3)中心原子为sp3杂化的极性分子
(4)中心原子为sp2杂化的极性分子
(5)既有极性键又有非极性键的非极性分子
查看习题详情和答案>>
根据要求用序号填空.
(1)属于原子晶体的化合物是
③
③
. (2)由极性分子构成的晶体是①⑤
①⑤
,属于分子晶体的单质是⑥
⑥
.(3)在一定条件下.受热熔化需克服共价键的是②③
②③
.II.在①H2O、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2、⑧C2H2分子中:
(1)全部以非极性键结合的非极性分子是
⑥
⑥
.(填序号 下同)(2)全部以极性键相结合,具有直线型结构的非极性分子是
④
④
.(3)中心原子为sp3杂化的极性分子
①②
①②
.(4)中心原子为sp2杂化的极性分子
⑦
⑦
.(5)既有极性键又有非极性键的非极性分子
⑧
⑧
.微粒A、B、C为分子,D和F为阳离子,E为阴离子,它们都含有l0个电子;B溶于A后所得的物质可电离出D和E;C是重要的化石能源.将A、B和含F离子的物质混合后可得D和一种白色沉淀.G3+离子与Ar原子的电子层结构相同.请回答:
(1)基态G原子的外围电子排布式是 .在A、B、C这三种分子中,属于非极性分子的有 (写化学式).
(2)下列有关B的说法中正确的是 .(填字母)
a.在配合物中可作为配体
b.该分子的稳定性与氢键有关
c.分子中各原子最外层均为8e-的稳定结构
d.含1molB的液体中有3mol氢键
(3)根据等电子体原理,D离子的空间构型是 ,其中心原子轨道的杂化类型是 .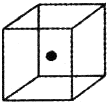
(4)构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,如图立方体中心的“●”表示该晶体中的一个原子,请在该立方体的顶点上用“●”表示出与之紧邻的原子.
(5)光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在 .(填字母)
a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.σ键 h.π键.
查看习题详情和答案>>
(1)基态G原子的外围电子排布式是
(2)下列有关B的说法中正确的是
a.在配合物中可作为配体
b.该分子的稳定性与氢键有关
c.分子中各原子最外层均为8e-的稳定结构
d.含1molB的液体中有3mol氢键
(3)根据等电子体原理,D离子的空间构型是

(4)构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,如图立方体中心的“●”表示该晶体中的一个原子,请在该立方体的顶点上用“●”表示出与之紧邻的原子.
(5)光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在
a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.σ键 h.π键.
锌是一种重要的金属,锌及其化合物有着广泛的应用.
①指出锌在周期表中的位置:第
②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式
③Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于

④如图2表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为
查看习题详情和答案>>
①指出锌在周期表中的位置:第
四
四
周期,第IIB
IIB
族,属于ds
ds
区.②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式
1s22s22p63s23p63d10或[Ar]3d10
1s22s22p63s23p63d10或[Ar]3d10
;葡萄糖分子中碳原子杂化方式有sp2、sp3
sp2、sp3
.③Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于
极性分子
极性分子
(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在图1中表示出[Zn(NH3)4]2+中Zn2+与N之间的化学键.
④如图2表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为
ZnX
ZnX
;该化合物晶体的熔点比干冰高
高
(填写“高”或“低”),原因是该化合物是原子晶体,而干冰是分子晶体
该化合物是原子晶体,而干冰是分子晶体
.