摘要:极性键:(1)概念: .(2)形成条件: .(3)共价键极性强弱比较依据:形成共价键的共用电子对偏向与偏离程度越大.键的极性就越强.试比较下列两组共价键的强弱:①H―H.H―F.H―O.H―N.H―C: ,②H―F.C―F.N―F.O―F.F―F: .
网址:http://m.1010jiajiao.com/timu_id_398887[举报]
现有短周期元素A、B、C、D、E五种元素,原子序数依次增大,A是元素周期表中所有元素中原子半径最小的;B、C同周期且基态原子的最外层皆有2个未成对电子;D元素的简单离子是本周期元素的简单离子中半径最小的;E原子M层中p电子数比s电子数多2个.请按要求回答下列问题:
(1)B元素基态原子的电子排布式为
 .
.
(2)写出两种由上述元素组成,含极性键的非极性分子的化学式
(3)写出D元素最高价氧化物水化物的电离方程式
(4)写出D、E形成的化合物与水反应的化学方程式
查看习题详情和答案>>
(1)B元素基态原子的电子排布式为
1s22s22p2
1s22s22p2
,A和C组成的含有非极性键的化合物的电子式为

(2)写出两种由上述元素组成,含极性键的非极性分子的化学式
CO2、CS2、CH4、C2H2、C6H6等
CO2、CS2、CH4、C2H2、C6H6等
(3)写出D元素最高价氧化物水化物的电离方程式
AlO2-+H++H2O?Al(OH)3?Al3+3OH-
AlO2-+H++H2O?Al(OH)3?Al3+3OH-
.(4)写出D、E形成的化合物与水反应的化学方程式
Al2S3+6H2O=2 Al(OH)3↓+3H2S↑
Al2S3+6H2O=2 Al(OH)3↓+3H2S↑
.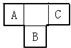 A、B、C、D、E为短周期元素,A、B、C在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.D与A同周期,其最高正价与最低负价代数和为零.A、E可形成AE3型分子,分子中只存在极性键.
A、B、C、D、E为短周期元素,A、B、C在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.D与A同周期,其最高正价与最低负价代数和为零.A、E可形成AE3型分子,分子中只存在极性键. (1)B元素在元素周期表中的位置是
第三周期VIA族
第三周期VIA族
.(2)C的离子结构示意图为




(3)由元素A、C及氢元素形成的化合物中含有的化学键的类型有
离子键、极性共价键
离子键、极性共价键
.(4)请设计一个实验来说明D与A的非金属性强弱(写出化学方程式即可)
2HNO3+Na2CO3=2NaNO3+H2O+CO2↑
(或其他合理方法)
(或其他合理方法)
2HNO3+Na2CO3=2NaNO3+H2O+CO2↑
(或其他合理方法)
.(或其他合理方法)
有A、B、C、D 4种短周期元素,它们的原子序数由A到D依次增大.
①D的氧化物分子式为DO,在D的氧化物中,氧的质量分数为40%,而且D的原子核中,质子数和中子数相等.
②A和B原子有相同的电子层数,A原子的最外层电子数是次外层电子数的2倍.
③B的阴离子与C的阳离子和Ne原子的电子层结构相同.在一定条件下0.1mol单质B2和0.2mol H2恰好完全反应,生成0.2mol氢化物.
④C的单质在点燃条件下与B的单质充分反应,可生成浅黄色固体,此生成物又可与A、B化合物反应生成B的单质.
(1)写出下列代号对应的元素符号:D
(2)写出AB2的结构式
(3)B、C两元素可形成两种不同的化合物,写出它们的电子式:
 、
、
 .
.
(4)A元素某氧化物与C元素某氧化物反应生成单质的化学方程式是
查看习题详情和答案>>
①D的氧化物分子式为DO,在D的氧化物中,氧的质量分数为40%,而且D的原子核中,质子数和中子数相等.
②A和B原子有相同的电子层数,A原子的最外层电子数是次外层电子数的2倍.
③B的阴离子与C的阳离子和Ne原子的电子层结构相同.在一定条件下0.1mol单质B2和0.2mol H2恰好完全反应,生成0.2mol氢化物.
④C的单质在点燃条件下与B的单质充分反应,可生成浅黄色固体,此生成物又可与A、B化合物反应生成B的单质.
(1)写出下列代号对应的元素符号:D
Mg
Mg
.(2)写出AB2的结构式
0=C=O
0=C=O
,所含化学键的类型B
B
.(填字母代号:A.离子键,B.极性键,C.非极性键)(3)B、C两元素可形成两种不同的化合物,写出它们的电子式:




(4)A元素某氧化物与C元素某氧化物反应生成单质的化学方程式是
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
.A、B、C、D、E都是短周期元素,原子序数依次增大;A原子中电子运动的轨道只有一种形状;B、C同周期,A、D同主族.D、B能形成两种离子化合物甲和乙,原子个数比分别为2:1和1:1;E元素原子的最外层电子数是其电子总数的
.根据以上信息回答下列问题:
(1)甲、乙中含有非极性键的物质的电子式是
 .
.
(2)E、C分别形成的氢化物稳定性大小关系是
(3)C和D的离子中,半径较小的是
 ,
,
 .
.
(4)写出B元素基态原子的轨道表示式
 .
.
(5)X是与E同主族的短周期元素,下表列出了X原子间各种共价键的键能:
通过计算说明X2中的
查看习题详情和答案>>
| 1 |
| 3 |
(1)甲、乙中含有非极性键的物质的电子式是


(2)E、C分别形成的氢化物稳定性大小关系是
HF>PH3
HF>PH3
.(用氢化物的化学式作答)(3)C和D的离子中,半径较小的是
Na+
Na+
(填离子符号).画出C和D的离子的结构示意图



(4)写出B元素基态原子的轨道表示式


(5)X是与E同主族的短周期元素,下表列出了X原子间各种共价键的键能:
| 键类型 | X-X | X=X | X≡X |
| 键能(kJ/mol) | 159 | 418 | 946 |
π键比σ键稳定
π键比σ键稳定
(填“σ键比π键稳定”或“π键比σ键稳定”).