摘要:常温 二.钠的化学性质 △ 1.与O2等非金属的反应: Na+O2 ── (切面很快变 ,Na2O加热时不稳定易转化成 ) Na+O2 ── ( 火焰,大量烟,生成 固体) 例1.mg金属钠与3.55g氯气恰好完全反应.生成g氯化钠.如将mg金属钠与O2恰好完全反应.生成物的质量可能为( ) A.g B.g D.g [思考]:钠置于空气中会发生一系列什么现象?发生了什么反应 Na+S – Na+Cl2-2.与H+反应: Na+H+ - 例2.将钠.镁.铝各0.3mol分别放入100ml 1mol/L的盐酸中.同温同压下产生的气体体积之比是 将钠.镁.铝各0.3mol分别放入100 mL1 mol·L-1盐酸中.同温同压下产生的气体的体积比是 A.1 : 2 : 3 B. 6 : 3 : 2 C. 3 : 1 : 1 D. 1 : 1 : 1
网址:http://m.1010jiajiao.com/timu_id_3987960[举报]
一次性筷子、一次性饭盒的安全受到社会的关注.专家介绍说,正规的一次性筷子所用的
原料都是质地较好的木材,不用特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为筷子看上去
白一些,他们常用硫磺进行熏蒸漂白,结果造成二氧化硫严重超标,同时硫磺中含铅、汞等重金属,也会
对人体造成铅中毒或汞中毒.
(1)“硫磺熏蒸”是应用二氧化硫的漂白性质,写出硫磺燃烧的化学方程式
(2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量.为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是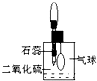 生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
(3)在制一次性筷子时有“抛光”程序:加入滑石粉和木签一起搅拌,起到干燥、打磨的作用,使筷子变得光滑,以免毛疵划人的口腔.已知滑石粉是一种含水的具有层状结构的硅酸盐矿物.其质量组成为MgO 31.88%,SiO263.37%,H2O 4.75%,其化学式为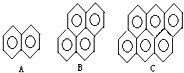
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒.有如右的一系列物质,则A的分子式为
查看习题详情和答案>>
原料都是质地较好的木材,不用特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为筷子看上去
白一些,他们常用硫磺进行熏蒸漂白,结果造成二氧化硫严重超标,同时硫磺中含铅、汞等重金属,也会
对人体造成铅中毒或汞中毒.
(1)“硫磺熏蒸”是应用二氧化硫的漂白性质,写出硫磺燃烧的化学方程式
S+O2
SO2
| ||
S+O2
SO2
| ||
(2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量.为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是
紫色石蕊试液变红、气球鼓胀起来
紫色石蕊试液变红、气球鼓胀起来
;为比较SO2 和CO2溶解性的大小,某学生采取同样的装置和操作,能说明SO2在水中的溶解性大于CO2在水中溶解性的实验现象是SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度
SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度
.某学 生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色)
品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色)
,接着向溶液中加入足量氯水,实验现象为 先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液)
先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液)
,再滴加BaCl2溶液,实验现象为生成白色沉淀(BaSO4)
生成白色沉淀(BaSO4)
.(3)在制一次性筷子时有“抛光”程序:加入滑石粉和木签一起搅拌,起到干燥、打磨的作用,使筷子变得光滑,以免毛疵划人的口腔.已知滑石粉是一种含水的具有层状结构的硅酸盐矿物.其质量组成为MgO 31.88%,SiO263.37%,H2O 4.75%,其化学式为
Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O
Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O
.
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒.有如右的一系列物质,则A的分子式为
C10H8
C10H8
,A、B、C可以互称同系物吗?为什么?不能
不能
因为A、B、C相差n个C6H2,不是n个CH2
因为A、B、C相差n个C6H2,不是n个CH2
.该系列化合物里碳的最大质量分数为97.3%
97.3%
;若E是A的一个氢原子被羟基取代的产物,预测E可能具有哪些化学性质(至少举2条)E能与溴水发生取代反应、
E能与溴水发生取代反应、
E与FeCl3能发生显色反应、E能和碳酸钠溶液反应
E与FeCl3能发生显色反应、E能和碳酸钠溶液反应
.(2010?潮州二模)Ⅰ.某学校探究性学习小组对84消毒液(有效成份:NaClO溶液)的制备与性质等进行以下探究.
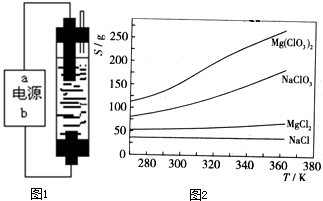
甲同学:为制备84消毒液,制作了一种家用环保型消毒液发生器,设计了如图1所示的装置,用石墨作电极电解饱和氯化钠.请填空:
(1)若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源的a极名称为
(2)用图示的装置电解饱和食盐水制备84消毒液(NaClO溶液)的离子方程式为
乙同学:从某超市中查询到某品牌消毒液包装说明的部分内容摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L.可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用.切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品.本品须密封,置阴凉暗处保存.
请完成以下实验探究过程:
阅读材料,根据学过的知识判断问题:
(3)室温条件下,该消毒液(NaClO)溶液的pH>7,原因是(用离子方程式表示)
(4)查得弱酸的电离常数:H2CO3K1=4.4×10-7,K2=4.7×10-11;HClO K=3×10-8.
从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示):
Ⅱ.Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3═Mg(ClO3)2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如图2所示:
①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因:
②按①中条件进行制备实验.在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:
查看习题详情和答案>>
甲同学:为制备84消毒液,制作了一种家用环保型消毒液发生器,设计了如图1所示的装置,用石墨作电极电解饱和氯化钠.请填空:

(1)若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源的a极名称为
负
负
极(填“正”、“负”),连接a极的电极反应式为2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-
2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-
.(2)用图示的装置电解饱和食盐水制备84消毒液(NaClO溶液)的离子方程式为
Cl-+H2O
ClO-+H2↑或2Cl-+2H2O
2OH-+H2↑+Cl2↑、Cl2+2OH-=ClO-+Cl-+H2O
| ||
| ||
Cl-+H2O
ClO-+H2↑或2Cl-+2H2O
2OH-+H2↑+Cl2↑、Cl2+2OH-=ClO-+Cl-+H2O
.
| ||
| ||
乙同学:从某超市中查询到某品牌消毒液包装说明的部分内容摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L.可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用.切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品.本品须密封,置阴凉暗处保存.
请完成以下实验探究过程:
阅读材料,根据学过的知识判断问题:
(3)室温条件下,该消毒液(NaClO)溶液的pH>7,原因是(用离子方程式表示)
ClO-+H2O?HClO+OH-
ClO-+H2O?HClO+OH-
.(4)查得弱酸的电离常数:H2CO3K1=4.4×10-7,K2=4.7×10-11;HClO K=3×10-8.
从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示):
NaClO+CO2+H2O=NaHCO3+HClO、2HClO
2HCl+O2↑
| ||
NaClO+CO2+H2O=NaHCO3+HClO、2HClO
2HCl+O2↑
.
| ||
Ⅱ.Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3═Mg(ClO3)2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如图2所示:
①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因:
在某一温度时,NaCl最先达到饱和析出,Mg(ClO3)2的溶解度随温度变化的最大,NaCl的溶解度与其他物质的溶解度有一定的差别
在某一温度时,NaCl最先达到饱和析出,Mg(ClO3)2的溶解度随温度变化的最大,NaCl的溶解度与其他物质的溶解度有一定的差别
.②按①中条件进行制备实验.在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:
降温前,溶液中NaCl已达饱和,降温过程中,NaCl溶解度会略为降低,会有少量晶体析出
降温前,溶液中NaCl已达饱和,降温过程中,NaCl溶解度会略为降低,会有少量晶体析出
.已知:H2A的A2-可表示S2-、S
、S
、Si
或C
离子.
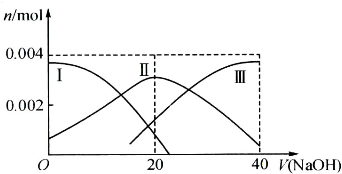
(1)常温下,向20mL 0.2mol?L-1 H2A溶液中滴加0.2mol?L-1 NaOH溶液.有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).请根据图示填空:
①当V(NaOH)=20mL时,溶液中离子浓度大小关系: ;
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水 (填“大”、“小”或“相等”),欲使NaHA溶液呈中性,可以向其中加入 .
(2)有关H2A的钠盐的热化学方程式如下:
①Na2SO4(s)═Na2S(s)+2O2(g)△H1=+1011.0kJ?mol-1;
②2C(s)+O2(g)═2CO(g)△H2=-221.0kJ?mol-1.
则Na2SO4(s)+4C(s)═Na2S(s)+4CO(g)△H3= kJ?mol-1;
工业上制备Na2S时往往要加入过量的碳,同时还要通入空气,目的有两个,其一是利用碳与氧气反应放出的热维持反应所需温度,其二是 .
(3)若H2A为硫酸:t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数KW= .
查看习题详情和答案>>
| O | 2- 4 |
| O | 2- 3 |
| O | 2- 3 |
| O | 2- 3 |
(1)常温下,向20mL 0.2mol?L-1 H2A溶液中滴加0.2mol?L-1 NaOH溶液.有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).请根据图示填空:

①当V(NaOH)=20mL时,溶液中离子浓度大小关系:
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水
(2)有关H2A的钠盐的热化学方程式如下:
①Na2SO4(s)═Na2S(s)+2O2(g)△H1=+1011.0kJ?mol-1;
②2C(s)+O2(g)═2CO(g)△H2=-221.0kJ?mol-1.
则Na2SO4(s)+4C(s)═Na2S(s)+4CO(g)△H3=
工业上制备Na2S时往往要加入过量的碳,同时还要通入空气,目的有两个,其一是利用碳与氧气反应放出的热维持反应所需温度,其二是
(3)若H2A为硫酸:t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数KW=
钠米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂.
(1)工业上二氧化钛的制备是:
I.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4.
II.将SiCl4分离,得到纯净的TiCl4.
III.在TiCl4中加水、加热,水解得到沉淀TiO2?xH2O.
IV.TiO2?Xh2O高温分解得到TiO2.

①TiCl4与SiCl4在常温下的状态是______.II中所采取的操作名称是______.
②III中反应的化学方程式是______.
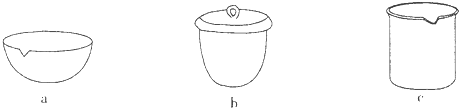
IV在实验室完成,应将TiO2?xH2O放在______(填仪器编号)中加热.

(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O,其过程大致如下:
a.O2→2O b.2O+H2O→2OH(羟基) c.OH+OH→H2O2
①b中破坏的是______(填“极性共价键”或“非极性共价键”).
②H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的______(填“氧化性”或“还原性”).
(3)某研究小组用下列装置模拟“生态马路”部分原理.(夹持装置已略去)
①如缓通入22.4L(已折算成标准状况)CO气体,结果NaOH溶液增重11g,则CO的转化率为______.
②当CO气体全部通入后,还要通一会儿空气,其目的是______.
查看习题详情和答案>>
(2010?朝阳区模拟)钠米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂.
(1)工业上二氧化钛的制备是:
I.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4.
II.将SiCl4分离,得到纯净的TiCl4.
III.在TiCl4中加水、加热,水解得到沉淀TiO2?xH2O.
IV.TiO2?Xh2O高温分解得到TiO2.
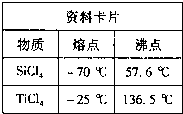
①TiCl4与SiCl4在常温下的状态是
②III中反应的化学方程式是
IV在实验室完成,应将TiO2?xH2O放在
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O,其过程大致如下:
a.O2→2O b.2O+H2O→2OH(羟基) c.OH+OH→H2O2
①b中破坏的是
②H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的
(3)某研究小组用下列装置模拟“生态马路”部分原理.(夹持装置已略去)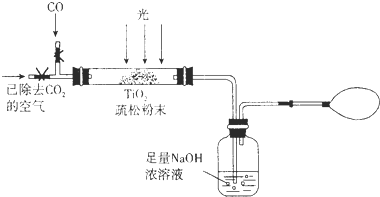
①如缓通入22.4L(已折算成标准状况)CO气体,结果NaOH溶液增重11g,则CO的转化率为
②当CO气体全部通入后,还要通一会儿空气,其目的是
查看习题详情和答案>>
(1)工业上二氧化钛的制备是:
I.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4.
II.将SiCl4分离,得到纯净的TiCl4.
III.在TiCl4中加水、加热,水解得到沉淀TiO2?xH2O.
IV.TiO2?Xh2O高温分解得到TiO2.

①TiCl4与SiCl4在常温下的状态是
液态
液态
.II中所采取的操作名称是蒸馏
蒸馏
.②III中反应的化学方程式是
TiCl4+(x+2)H2O
TiO2?xH2O↓+4HCl
| ||
TiCl4+(x+2)H2O
TiO2?xH2O↓+4HCl
.
| ||
IV在实验室完成,应将TiO2?xH2O放在
b
b
(填仪器编号)中加热.
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O,其过程大致如下:
a.O2→2O b.2O+H2O→2OH(羟基) c.OH+OH→H2O2
①b中破坏的是
极性共价键
极性共价键
(填“极性共价键”或“非极性共价键”).②H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的
氧化性
氧化性
(填“氧化性”或“还原性”).(3)某研究小组用下列装置模拟“生态马路”部分原理.(夹持装置已略去)

①如缓通入22.4L(已折算成标准状况)CO气体,结果NaOH溶液增重11g,则CO的转化率为
25%
25%
.②当CO气体全部通入后,还要通一会儿空气,其目的是
将残留在装置中的CO2气体排出,被NaOH溶液吸收,减少误差
将残留在装置中的CO2气体排出,被NaOH溶液吸收,减少误差
.