摘要:7.已知NH4++AlO2-+2H2OAl(OH)3↓+NH3·H2O.向含有等物质的量的NH4+.Al3+.H+混合溶液中.慢慢滴加NaOH溶液.直至过量.并不断搅拌.依次发生了数个离子反应.则第三个离子反应是( ). A.H++OH-H2O B.Al3++3OH-Al(OH)3↓ C.Al(OH)3+OH-AlO2-+2H2O D.NH4++OH-NH3·H2O [解析]选D.通常来说溶液中的离子反应以H+与OH-间的中和反应速率最快.其它则需根据某些原理分析.故第一个反应为中和反应:H++OH-H2O.第二个反应为:Al3++3OH-Al(OH)3↓.但发生第二个反应后.又出现两性Al(OH)3与NH4+何者优先反应的问题.若Al(OH)3优先与OH-反应.则产物AlO2-能够与NH4+又发生题给的双水解反应而不能共存又变回Al(OH)3.故第三个反应为NH4++OH-NH3·H2O.最后一个离子反应为Al(OH)3+OH-AlO2-+2H2O.
网址:http://m.1010jiajiao.com/timu_id_3977240[举报]
(2010?娄底模拟)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂.工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4).
湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4
下列有关说法不正确的是( )
湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4
下列有关说法不正确的是( )
查看习题详情和答案>>
 (2011?宝鸡模拟)化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如图所示;
(2011?宝鸡模拟)化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如图所示;现提供以下化学键的键能:P-P 198KJ?mol-1、P-O 360kJ?mol-1、氧气分子内氧原子间的键能为498kJ?mol-1则P4+3O2═P4O6的反应热△H为( )
查看习题详情和答案>>
(2010?惠州模拟)某同学对Cu的常见化合物的性质进行实验探究,研究的问题和过程如下:
①在周期表中Cu和Al位置比较接近,Al(OH)3具有两性,Cu(OH)2是否也有两性?
②通常情况下,+2价Fe不如十3价Fe稳定,十l价Cu也一定不如+2价Cu稳定吗?
③CuO有氧化性,能被H2、CO还原,CuO也能被NH3还原吗?
(I)为探究问题①,除Cu(OH)2外必须选用的试剂为
a、稀H2SO4 b、浓的NaOH溶液 c、浓氨水 (NH3.H2O)
(II)为探究问题②,进行如下实验:
(1)将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末,该反应的化学方程式为
(2)向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,+1价Cu比+2价Cu更
(III)为解决问题③,他设计了如下实验(夹持装置未画):
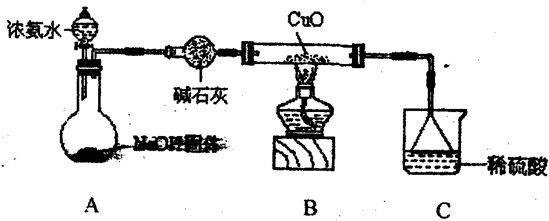
装置B中NH3和CuO反应生成铜,同时生成一种无污染的气体,反应的化学方程式为
查看习题详情和答案>>
①在周期表中Cu和Al位置比较接近,Al(OH)3具有两性,Cu(OH)2是否也有两性?
②通常情况下,+2价Fe不如十3价Fe稳定,十l价Cu也一定不如+2价Cu稳定吗?
③CuO有氧化性,能被H2、CO还原,CuO也能被NH3还原吗?
(I)为探究问题①,除Cu(OH)2外必须选用的试剂为
a、b
a、b
(填序号):a、稀H2SO4 b、浓的NaOH溶液 c、浓氨水 (NH3.H2O)
(II)为探究问题②,进行如下实验:
(1)将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末,该反应的化学方程式为
4CuO
2Cu2O+O2↑
| ||
4CuO
2Cu2O+O2↑
.该反应说明:在高温条件下,十l价的Cu比十2价Cu更
| ||
稳定
稳定
(填“稳定”或“不稳定”).(2)向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,+1价Cu比+2价Cu更
不稳定
不稳定
(填“稳定”或“不稳定”).(III)为解决问题③,他设计了如下实验(夹持装置未画):

装置B中NH3和CuO反应生成铜,同时生成一种无污染的气体,反应的化学方程式为
3CuO+2NH3
N2 ↑+3Cu+3H2O
| ||
3CuO+2NH3
N2 ↑+3Cu+3H2O
,说明CuO能够被NH3还原.装置C的作用:
| ||
充分吸收反应多余的NH3,并防止倒吸现象
充分吸收反应多余的NH3,并防止倒吸现象
.