网址:http://m.1010jiajiao.com/timu_id_3971918[举报]
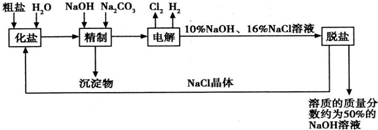
请回答下列问题:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为
(2)粗盐中含Ca2+、Mg2+等杂质.精制过程中发生反应的离子方程式为
(3)为有效除去Ca2+、Mg2+和S
| O | 2- 4 |
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3,
C.先加钡试剂,后加NaOH,再加Na2CO3
(4)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(5)采用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜法电解食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学反应方程式为
| ||
| ||
(1)电解过程中发生反应的化学方程式是
(2)氢气在电解池的
(3)HCl合成反应中保持过量的气体是
(4)利用HCl合成时放出的热量来产生水蒸汽,用于NaOH溶液的蒸发,这样做的优点是
(5)检验NaOH产品中是否含有NaCl的实验方案是
(6)为测定含少量NaCl的NaOH产品的纯度,某同学准确称取产品4.000g,溶于水配成1000mL溶液,用0.1000mol/L的标准盐酸滴定.实验记录的数据如下表:
| 实验次数 | 待测液体积(mL) | 标准盐酸溶液体积(mL) |
| 1 | 20.00 | 21.32 |
| 2 | 20.00 | 19.45 |
| 3 | 20.00 | 19.35 |
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下: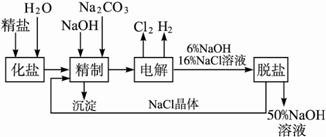
依据上图,完成下列填空:
(1)工业食盐中含Ca2+、Mg2+等杂质,精制过程中发生反应的离子方程式为 ___________________________,___________________________。
(2)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________________。
,该钡试剂可以是________________。
a.Ba(OH)2?b.Ba(NO3)2?c.BaCl2
(3)为有效除去Ca2+、Mg2+、![]() ,加入试剂的合理顺序为____________。
,加入试剂的合理顺序为____________。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______________、冷却、______________除去NaCl。(填写操作名称)
(5)电解食盐水时,总的反应方程式为____________________________。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为____________________________。
查看习题详情和答案>>氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下: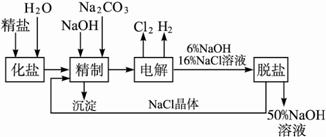
依据上图,完成下列填空:
(1)工业食盐中含Ca2+、Mg2+等杂质,精制过程中发生反应的离子方程式为 ___________________________,___________________________。
(2)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________________。
,该钡试剂可以是________________。
a.Ba(OH)2?b.Ba(NO3)2?c.BaCl2
(3)为有效除去Ca2+、Mg2+、![]() ,加入试剂的合理顺序为____________。
,加入试剂的合理顺序为____________。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______________、冷却、______________除去NaCl。(填写操作名称)
(5)电解食盐水时,总的反应方程式为____________________________。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为____________________________。
查看习题详情和答案>>