网址:http://m.1010jiajiao.com/timu_id_3968100[举报]
| A、二氧化硫可广泛用于食品的漂白 | B、煤经过气化和液化等物理变化可以转化为清洁燃料 | C、淀粉、油脂和蛋白质都是天然高分子化合物,都能发生水解反应 | D、利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
化学与生活密切相关,下列说法正确的是
A.二氧化硫可广泛用于食品的漂白
B.煤经过气化和液化等物理变化可以转化为清洁燃料
C.淀粉、油脂和蛋白质都是天然高分子化合物,都能发生水解反应
D.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程
查看习题详情和答案>>
化学与生活密切相关,下列说法正确的是
| A.二氧化硫可广泛用于食品的漂白 |
| B.煤经过气化和液化等物理变化可以转化为清洁燃料 |
| C.淀粉、油脂和蛋白质都是天然高分子化合物,都能发生水解反应 |
| D.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
(1)化学与材料密切相关,材料科学的发展和新材料的开发都离不开化学.
①下列硅酸盐产品的生产原料中,不需要石灰石的是
a.玻璃 b.水泥 c.陶瓷
②在快中子反应堆中得以广泛应用的钠钾合金在常温下呈液态,这个事实说明合金的熔点比其成分金属的熔点
a.高 b.低 c.可能高也可能低
③下列物质中,属于合成有机高分子材料的是
a.聚苯乙烯 b.棉花 c.光导纤维
(2)新年伊始,全国许多城市启用新的环境空气质量指数来评价空气质量,环境质量的好坏越来越引起全社会的关注.
①空气污染指数API表明了空气的质量.空气污染指数是根据空气中二氧化硫、二氧化氮和
②自来水厂常用漂白粉、液氯、二氧化氯、臭氧等作为消毒剂,杀灭水中的细菌.液氯注入水中后,能杀死水中细菌的物质是
③向燃煤中加入石灰石作脱硫剂,可大大减少SO2的排放及酸雨的发生,用这种方法最终可将煤中的硫转化为
硝酸型酸雨的形成主要是由汽车排放的尾气所致,汽车尾气中的氮氧化物可以用氨气来处理.例如,氨气与二氧化氮反应生成的物质均是对空气无污染的物质,请写出此时氨气与二氧化氮反应的化学方程式:
(3)合理饮食和正确用药,是人体健康的重要保证.
①合理食用加碘盐是防止缺碘性疾病的有效方法之一,在人体必需元素中,碘属于
抗酸药可治疗胃酸过多的原因是这类药物中含有的一种或几种化学物质,能与胃里过多的
②纤维素被称为“第七营养素”,从化学成分看,纤维素属于
③亚硝酸钠(NaNO2)有很强的毒性,其外观似食盐、有咸味,误食会中毒,在酸性溶液中、微热时亚硝酸钠能产生NO和NO2气等.请写出鉴别亚硝酸钠和氯化钠的实验方法和现象:
Ⅰ)纯净的过氧化钙(CaO2)难溶于水、乙醇,常温下较为稳定。CaO2·8H2O在0℃时稳定,加热至130℃时逐渐变为无水CaO2。在实验室可用钙盐制取CaO2·8H2O,再经脱水制得CaO2。其制备过程如下:
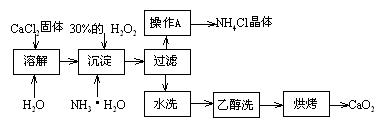
根据以上信息,回答下列问题:
⑴用上述方法制取CaO2·8H2O的化学方程式是_▲_;
⑵测定产品中CaO2的含量的实验步骤是(己知:I2+2S2O32-=2I-+S4O62-):
第一步:准确称取ag产品于锥形瓶中,加入适量蒸馏水和过量的bgKI品体,再滴入适量2mol·L-1的H2SO4溶液,充分反应:
第二步:向上述锥形瓶中加入几滴淀粉溶液:
第三步:逐滴加入浓度为cmol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液VmL。
①第三步反应完全时的现象为 ▲ ;
②产品中CaO2的质量分数为 ▲ (用字母表示);
③某同学经实验测得产品中CaO2的质量分数偏高,造成偏高的原因是(测定过程中由操作产生的误差忽略不计,用离子方程式表示) ▲ 。
Ⅱ)硫酸铜是一种重要的化工原料,工业上常用硫酸为原料来制备硫酸铜。
⑴工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源。
①为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4。写出该反应的化学方程式_ ▲ _;实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是 ▲ 。
②氯化焙烧工艺是将废渣用氯化钙水溶液调和、成球、高温焙烧,废渣中SiO2与CaCl2等在高温下反应放出HCl,HCl与金属氧化物等反应生成氯化物。反应生成的各金属氯化物以气态形式逸出,进而回收有色金属和回返氯化钙溶液。写出氯化焙烧工艺中生成HCl的化学方程式 ▲ 。
⑵测定硫酸铜品体中结品水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重:
步骤5: ▲ ;
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数。
请完成实验步骤5。
(3)已知硫酸铜晶体受热可以逐步失去结晶水,温度升高还可以分解生成铜的氧化物。取25.0gCuSO4·5H2O晶体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示:
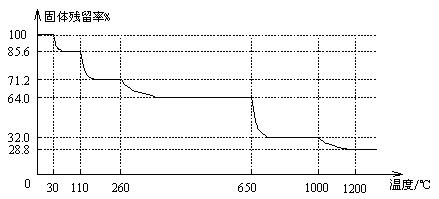
在110℃时所得固体的成分为 ▲ ;在1200℃并恒温1小时,反应所得气态产物除去水后,物质的量为 ▲ 。(填字母)
A.0mol B.0.1mol C.0.125mol D.大于0.125mol
查看习题详情和答案>>