摘要:Na2S2O3 + H2SO4 . CaO+SiO2.KOH+CO2. KHCO3分解.Ba(OH)2·8H2O + NH4Cl
网址:http://m.1010jiajiao.com/timu_id_3967865[举报]
Na2S2O3溶液跟稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O.下列各组实验中,溶液中最先变浑浊的是( )
| 反应温度(℃) | 反应物 | H2O | ||||
| Na2S2O3 | H2SO4 | V(mL) | ||||
| V(mL) | c(mol/L) | V(mL) | c(mol/L) | |||
| A | 10 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
| A、A | B、B | C、C | D、D |
(2012?江苏一模)氯化铁是常见的水处理剂,工业上制备无水FeCl3的一种工艺如下:
(1)试写出吸收塔中反应的离子方程式:
(2)六水合氯化铁在水中的溶解度如下:
从FeCl3溶液制得FeCl3?6H2O晶体的操作步骤是:加入少量盐酸、
(3)常温下,若溶液的pH控制不当会使Fe3+沉淀,pH=4时,溶液中c(Fe3+)=
(常温下Ksp[Fe(OH)3]=2.6×10-39).
(4)FeCl3的质量分数通常可用碘量法测定:称取mg无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用c mol?L-1 Na2S2O3溶液滴定用去V mL.(已知:I2+2S2O32-═2I-+S4O62-)
①滴定终点的现象是:
②求样品中氯化铁的质量分数(写出计算过程).
查看习题详情和答案>>

(1)试写出吸收塔中反应的离子方程式:
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(2)六水合氯化铁在水中的溶解度如下:
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
蒸发浓缩
蒸发浓缩
、冷却结晶
冷却结晶
、过滤、洗涤、干燥.(3)常温下,若溶液的pH控制不当会使Fe3+沉淀,pH=4时,溶液中c(Fe3+)=
2.6×10-9 mol?L-1
2.6×10-9 mol?L-1
mol?L-1.(常温下Ksp[Fe(OH)3]=2.6×10-39).
(4)FeCl3的质量分数通常可用碘量法测定:称取mg无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用c mol?L-1 Na2S2O3溶液滴定用去V mL.(已知:I2+2S2O32-═2I-+S4O62-)
①滴定终点的现象是:
滴入最后一滴,溶液颜色由蓝色变为无色,且半分钟内不变色
滴入最后一滴,溶液颜色由蓝色变为无色,且半分钟内不变色
.②求样品中氯化铁的质量分数(写出计算过程).
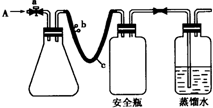 (2012?南通模拟)实验室用下列方法测定某水样中O2的含量.
(2012?南通模拟)实验室用下列方法测定某水样中O2的含量.(1)实验原理
用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为
2Mn2++O2+4OH-=2MnO(OH)2
2Mn2++O2+4OH-=2MnO(OH)2
.再用I-将生成的MnO(OH)2还原为Mn2+,反应的离子方程式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O.然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为:I2+2Na2S2O3=2NaI+Na2S4O6.(2)实验步骤
①打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是
赶走装置内空气,避免空气中的O2的干扰
赶走装置内空气,避免空气中的O2的干扰
;②用注射器抽取某水样20.00mL从A 处注入锥形瓶;
③再分别从A 处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A 处注入足量NaI溶液,并用稀H2SO4溶液调节pH至接近中性;
⑥
重复④的操作
重复④的操作
;⑦取下锥形瓶,向其中加入2~3滴
淀粉溶液
淀粉溶液
作指示剂;⑧用0.005mol?L-1Na2S2O3 滴定至终点.
(3)数据分析
①若滴定过程中消耗的Na2S2O3 标准溶液体积为3.90mL,则此水样中氧(O2)的含量为
7.8mg?L-1
7.8mg?L-1
(单位:mg?L-1).②若未用Na2S2O3 标准溶液润洗滴定管,则测得水样中O2的含量将
偏大
偏大
(填“偏大”、“偏小”或“不变”).③步骤⑤中加入适量的H2SO4使溶液接近中性,其原因是
加入稀H2SO4使MnO(OH)2充分转化为Mn2+,但加入稀H2SO4的量时不宜过多,否则后续滴定过程中Na2S2O3与过量的酸反应导致消耗的Na2S2O3溶液偏大
加入稀H2SO4使MnO(OH)2充分转化为Mn2+,但加入稀H2SO4的量时不宜过多,否则后续滴定过程中Na2S2O3与过量的酸反应导致消耗的Na2S2O3溶液偏大
.I、实验室可利用下列步骤通过“化学放大”来测定极稀的碘化物溶液中I-的浓度:①在中性或弱酸性溶液中,用溴将试样中的I-完全氧化,生成溴化物和碘酸盐,再煮沸以除去过量的Br2;②将所得溶液冷却至室温,加入足量的KI溶液和稀硫酸,充分反应后加入CCl4足量(假设作用完全),再用仪器A将油层分出;③油层用肼(H2N-NH2)的水溶液将CCl4中的I2还原为I-,并进入水溶液中;④水溶液按①法处理;⑤将④所得溶液冷却后加入适量KI溶液并用H2SO4酸化;⑥将⑤所得到溶液取一定量用Na2S2O3标准溶液进行滴定,得出本步骤后溶液中I-的浓度,以此求出原稀溶液中I-浓度,滴定时的反应为:2Na2S2O3+I2=Na2S4O6+2NaI.试回答:
(1)仪器A的名称 ,如果CCl4用汽油代替,在将油层分出时进行的操作为 .
(2)如果某试管中有上下两层,均呈无色,采取什么办法判断哪一层是水溶液? .
(3)写出离子方程式:步骤① ;步骤⑤ .
(4)滴定时, 手控制活塞, 手摇动锥形瓶.
II、Ag+浓度为0.100mol?L-1的溶液5mL,加入等物质的量的某碱金属盐,充分反应后生成卤化物沉淀,经过滤、洗涤后在200W灯泡下烘干,得到1.297×10-2 g固体.
(5)如果卤化物沉淀为AgX,则其物质的量为 mol,根据数据分析上述沉淀是否为AgX沉淀: (填“是”或“不是”);若为AgX沉淀,则它的化学式为 (若不为AgX沉淀,则此空不填).
(6)如果卤化物沉淀为碱金属卤化物,其摩尔质量为 (计算结果保留整数),根据分析,它的化学式为 .
查看习题详情和答案>>
(1)仪器A的名称
(2)如果某试管中有上下两层,均呈无色,采取什么办法判断哪一层是水溶液?
(3)写出离子方程式:步骤①
(4)滴定时,
II、Ag+浓度为0.100mol?L-1的溶液5mL,加入等物质的量的某碱金属盐,充分反应后生成卤化物沉淀,经过滤、洗涤后在200W灯泡下烘干,得到1.297×10-2 g固体.
(5)如果卤化物沉淀为AgX,则其物质的量为
(6)如果卤化物沉淀为碱金属卤化物,其摩尔质量为