摘要:从铝土矿中提取铝的工艺流程为: 写出反应的化学方程式: ① ② ③ ④
网址:http://m.1010jiajiao.com/timu_id_3957195[举报]
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

请回答下列问题:
(1)Fe的原子序数为26,Fe位于元素周期表中第
(2)流程甲加入盐酸后生成Al3+的离子方程式为
(3)滤液E中溶质的主要成份是
(4)写出检验滤液B中是否含Fe3+离子的方法:
查看习题详情和答案>>

请回答下列问题:
(1)Fe的原子序数为26,Fe位于元素周期表中第
四
四
周期,第VIII
VIII
族.(2)流程甲加入盐酸后生成Al3+的离子方程式为
Al2O3+6H+═2Al3++3H2O
Al2O3+6H+═2Al3++3H2O
;流程乙加入烧碱后生成SiO32-的离子方程式为SiO2+2OH-═SiO32-+H2O
SiO2+2OH-═SiO32-+H2O
.(3)滤液E中溶质的主要成份是
NaHCO3
NaHCO3
(填化学式),写出该溶液的一种用途:制纯碱或做发酵粉等
制纯碱或做发酵粉等
.(4)写出检验滤液B中是否含Fe3+离子的方法:
取少量滤液B于试管中,向其中加入硫氰化钾溶液,溶液变红色,说明滤液中含Fe3+,溶液不变红色,说明滤液中不含Fe3+
取少量滤液B于试管中,向其中加入硫氰化钾溶液,溶液变红色,说明滤液中含Fe3+,溶液不变红色,说明滤液中不含Fe3+
.从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取Al2O3两种工艺的流程如下:

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为
(2)流程乙加入烧碱后生成SiO32-的离子方程式为
(3)流程甲滤液D中通入过量CO2的化学方程式为
(4)“通入过量CO2”能否改用盐酸
(5)滤液E、K中溶质的主要成份是
查看习题详情和答案>>

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为
Al2O3+6H+=2Al3++3H2O
Al2O3+6H+=2Al3++3H2O
.(2)流程乙加入烧碱后生成SiO32-的离子方程式为
SiO2+2OH-=SiO32-+H2O
SiO2+2OH-=SiO32-+H2O
.(3)流程甲滤液D中通入过量CO2的化学方程式为
NaA1O2+CO2+2H2O=A1(OH)3↓+NaHCO3
NaA1O2+CO2+2H2O=A1(OH)3↓+NaHCO3
.(4)“通入过量CO2”能否改用盐酸
不能
不能
,原因是A1(OH)3沉淀会溶于过量的盐酸中
A1(OH)3沉淀会溶于过量的盐酸中
.(5)滤液E、K中溶质的主要成份是
NaHCO3
NaHCO3
(填化学式),写出该溶液的一种用途制纯碱或做发酵粉等
制纯碱或做发酵粉等
.
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
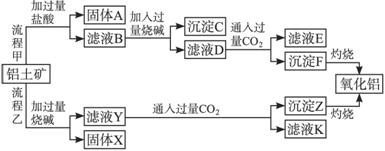
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为______________________________。
(2)流程乙加入烧碱后生成![]() 的离子方程式为_____________________________。
的离子方程式为_____________________________。
(3)验证滤液B含Fe3+,可取少量滤液并加入_______________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是_______________(填化学式),写出该溶质的一种用途_______________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12。取适量的滤液B,加入一定量的烧碱至达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________。
查看习题详情和答案>>

