摘要:2P + 3Cl2 2PCl3 2P + 5Cl2======2PCl5
网址:http://m.1010jiajiao.com/timu_id_3947571[举报]
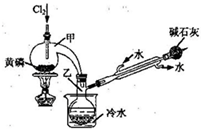 (2011?南京二模)PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:
(2011?南京二模)PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:| 熔点/℃ | 沸点/℃℃℃ | 密度/g?cm-3 | 其他 | |||||||||
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2
| ||||||||
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 | ||||||||
| POCl3 | 2 | 105 3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
①向甲中通入干燥的Cl2之前,需先通入一段时间CO2,目的是
排尽装置中的空气,防止生成的PCl3与空气中的O2和H2O反应
排尽装置中的空气,防止生成的PCl3与空气中的O2和H2O反应
.②实验过程中,应控制
氯气的流量
氯气的流量
,以减少PCl5的生成.③蒸馏烧瓶乙中得到的粗产品含有POCl3、PCl5
等.加入黄磷加热除去PCl5后,通过
蒸馏
蒸馏
(填实验操作名称),即可得到PCl,纯品.(2)已知:
a.H3PO3+H2O+I2?H3PO4+2HI
b.(NH4)3BO3,溶液可与HI和H3PO4反应生成H3BO3
c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3=Na2S4O6+2NaI
①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取mg产品,水解完全后在500mL容量瓶中定容;
步骤2:从容量瓶中移取25.00mL溶液置于碘量瓶中;
步骤3:准确加入c1mol?L-1碘溶液V1 mL(过量),再
迅速加入足量(NH4)3BO3溶液
迅速加入足量(NH4)3BO3溶液
;步骤4:
加入淀粉溶液,立即用Na2S2O3标准溶液回滴过量的碘
加入淀粉溶液,立即用Na2S2O3标准溶液回滴过量的碘
;滴至终点时消耗耗c2mol?L-1Na2S2O3溶液V2mL;②根据上述数据,该产品中PCl3的质量分数为2.75(c1v1-
| ||
| m |
2.75(c1v1-
| ||
| m |