网址:http://m.1010jiajiao.com/timu_id_385176[举报]
将化学知识的系统化,有助于对化学问题的进一步认识。请你参与下列关于化学反应的讨论。
问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在上图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系。
问题2:不同化学反应进行的快慢和程度千差万别。反应的快慢和程度是化工生产考虑的两个重要因素。请你按照表中要求完成下表(填写内容不能重复)。
| 序号 | 实际生产中采取的措施 | 工业生产实例(写名称) |
| (1) | 通过增大压强提高原料转化率 | |
| (2) | 使用催化剂增大反应的速率 |
问题3:化学反应中均伴随着能量的变化。如果一个化学反应中,反应物的总能量和生成物
的总能量有如图所示的关系,则该反应过程中的能量变化是 。
 已知热化学方程式为:
已知热化学方程式为:
C(g) + O2(g)= CO2 (g) △H= ―393.5KJ/mol
H2 (g) + 1/2O2 (g)= H2O (l) △H= ―285.8KJ/mol
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是 (保留1位小数)。
问题4:化学反应的发生是有条件的。反应物相同,反应的条件不同,反应的原理不同。
如:4Na+O2=2Na2O 2Na+O2![]() Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同: 。
Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同: 。
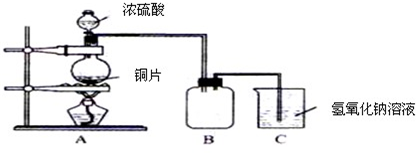
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整.
(2)实验中他们取6.4g 铜片和12mL 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①写出铜跟浓硫酸反应的化学方程式:
| ||
| ||
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是:
A.铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(3)为定量测定余酸的物质的量浓度,甲学生进行了如下设计学生设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL,取20mL与锥形瓶中,滴入2~3滴甲基橙指示剂,用标准氢氧化钠溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),通过测出消耗氢氧化钠溶液的体积来求余酸的物质的量浓度.假定反应前后烧瓶中溶液的体积不变,你认为他设计的实验方案能否求得余酸的物质的量浓度
(4)现已确认,SO2和NOx的排放是造成酸沉降的两大罪魁祸首.汽车排放的尾气中含有未燃烧充分的CH、以及N2、CO2、NO、CO等.有人设计利用反应2NO+2CO
 N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
I.催化重整制氢。以甲醇为例,反应制氢气的一般途径有:
CH3OH(l)=2H2(g)+CO(g) △H1=+128 kJ./mol;
CH3OH(l) +H2O(l)=3H2(g) +CO2(g) △H2=a kJ/mol;
已知:H2(g)+1/2O2(g)=H2O(l) △H=-286 kJ/mol。
为求得△H2,还要知道____ 的燃烧热,若其燃烧热为△H3= -283 kJ/mol,则 △H2=____。
Ⅱ金属置换制氢
(1)研究表明,刚切割的金属表面具有很高的反应活性。 当铝或铝合金在水中被切割或碾碎的时候,可以持续地释放出氢气。使用铝与水反应制氢气比使用其他活泼金属与水反应制氢气的优点有:
①价廉,成本较低; ②____________________。
(2)利用天然气重整得到的CO、H2混合气对金属氧化物进行还原,然后将金属与水反应放出氢气,由此达成一个良性循环。根据高中所学的知识合理测该金属单质,并写出该金属在加热的条件下与水蒸气反应的化学方程式_______________________
Ⅲ太阳能制氢利用光能分解水必须要有催化剂的参与。下列有关催化剂的说法止确的是________
A使用高效催化剂分解水制得H2的同时还可以获得能量
B使刚高效催化剂后常温下水可以自发分解
C硅胶具有多孔结构,有较大的表面积,常用做催化剂的载体
D对于可逆反应,催化剂在增大正反应速率的同时也增大逆反应速率,同时使化学平衡常数增大
Ⅵ配位氢化物制氢在硼氢化钠(NaBH4)水溶液中加入特定催化剂后,可以迅速地发生水解反应生成偏硼酸钠和氢气。
请写出此水解反应的化学方程式____________________。
将无水偏硼酸钠、氢化镁(MgH2)放入研磨设备中,通入缸气或氢气并保持压强100~500 kPa研磨0.5-4h,即可得到硼氢化钠。研磨过程中需要通入氲气或氢气并保持压强100~500kPa的目的是_____________
(08浙江舟山中学月考) 将化学知识的系统化,有助于对化学问题的进一步认识。请你参与。
问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在右图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系(用一个圆圈表示一类反应)。
问题2:不同化学反应进行的快慢和程度千差万别。反应的快慢和程度是化工生产考虑的两个重要因素。请你按照表中要求完成下表(填写内容不能重复)。
序号 | 实际生产中采取的措施 | 工业生产实例(写名称) |
(1) | 通过增大压强提高原料转化率 |
|
(2) | 使用催化剂增大反应的速率 |
|
问题3:化学反应中均伴随着能量的变化。如果一个化学反应中,反应物的总能量和生成物的总能量有如图所示的关系,则该反应过程中的能量变化是 (填放热或吸热)。

已知热化学方程式为:
C(s) + O2(g)= CO2 (g) △H= ―393.5KJ?mol-1
H2 (g) + 1/2O2 (g)= H2O (l) △H= ―285.8KJ?mol-1
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是 :1(保留1位小数)。
问题4:化学反应的发生是有条件的。反应物相同,反应的条件不同,反应的原理不同。如:
4Na+O2=2Na2O 2Na+O2![]() Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用化学反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同:
Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用化学反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同:
查看习题详情和答案>>
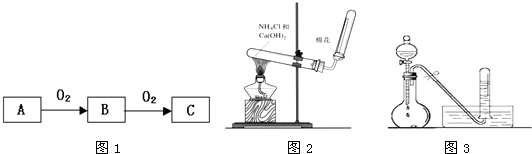
(1)若A是一种黄色单质固体,则B→C的化学方程式为
| 催化剂 |
| △ |
| 催化剂 |
| △ |
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体.如图2所示是实验室制取A气体的装置,请结合所学知识,回答下列问题:
①收集A的方法是
(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
②写出实验室制取A的化学方程式
| ||
| ||
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为
④试写出C与水反应的化学方程式