摘要: NO2-的不稳定性向NaNO2溶液中加酸.生成HNO2.HNO2不稳定.仅存在于冷的稀溶液中.微热甚至常温下也会分解.产生红棕色的NO2气体.NaNO2+H2SO4(稀)=NaHSO4+HNO2 2HNO2=NO↑+NO2↑+H2O
网址:http://m.1010jiajiao.com/timu_id_385170[举报]
亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解.
(1)写出亚硝酸的电离方程式: .
(2)在酸性条件下,当NaNO2与KI按物质的量之比1:1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为 (填化学式).
(3)要得到稳定的HNO2溶液,可以向冷冻的NaNO2浓溶液中加入或通入某种物质,下列物质不适合的是 (填字母).
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.磷酸
(4)碱性工业废水中的NO2-可用铝粉除去.已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3?H2O、H2O六种物质.
①写出上述反应的离子方程式: .
②发生上述反应后废水的pH将 (填“增大”、“减小”或“不变”).
(5)酸性工业废水中的NO2-可用尿素除去.尿素(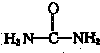 )与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为 g.
)与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为 g.
查看习题详情和答案>>
(1)写出亚硝酸的电离方程式:
(2)在酸性条件下,当NaNO2与KI按物质的量之比1:1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为
(3)要得到稳定的HNO2溶液,可以向冷冻的NaNO2浓溶液中加入或通入某种物质,下列物质不适合的是
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.磷酸
(4)碱性工业废水中的NO2-可用铝粉除去.已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3?H2O、H2O六种物质.
①写出上述反应的离子方程式:
②发生上述反应后废水的pH将
(5)酸性工业废水中的NO2-可用尿素除去.尿素(
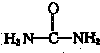 )与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为
)与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为