网址:http://m.1010jiajiao.com/timu_id_385161[举报]
下列说法中,正确的是()
①镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀
②钢铁表面常易锈蚀生成Fe2O3×nH2O
③锌和铁构成原电池时,铁作负极
④铅蓄电池中铜作负极PbO2作正极,两极浸到稀H2SO4中
- A.只有②④
- B.只有①③
- C.①②③
- D.①②③④
在稀硫酸与锌反应制取氢气的实验中,探究加人硫酸铜溶液的量对氢气生成速率的影响。实验中Zn粒过量且颗粒大小相同,饱和硫酸铜溶液用量0一4.0mL,保持溶液总体积为100.0mL,记录获得相同体积(336 mL,)的气体所需时间,实验结果如图所示(气体体积均转化为标况下)。据图分析,下列说法不正确的是
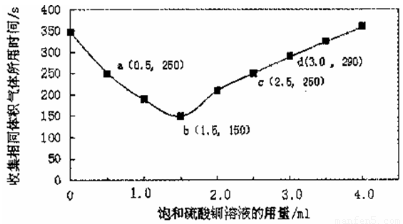
A.饱和硫酸铜溶液用量过多不利于更快收集氢气
B.a ,c两点对应的氢气生成速率相等
C.b点对应的反应速率为v( H2SO4)=1.0x10-3mol·L -1 ·s-1
D.d点没有构成原电池,反应速率减慢
查看习题详情和答案>>
“铝和氯化铜溶液反应”实验中预料之外现象的研究
化学实验中预料之外的现象往往包含我们还没有认识的事物规律。下面是某同学进行“铝和氯化铜溶液反应”实验时观察到的预料之外的现象:
①铝丝表面附上的铜没有紧密吸附在铝丝的表面而是呈蓬松的海绵状;②反应一段时间后有大量气泡逸出,且在一段时间内气泡越来越快,经点燃能发出爆鸣声,证明是氢气。
“科学研究还离不开合理的猜想和假设。”该同学先从理论上猜想铝丝表面产生氢气的多种可能原因,再设计实验验证自己的猜想。
实验操作及现象记录:
取4根去油去锈的铝丝为A组直接和下列溶液反应,4根下半截缠上细铜丝的铝丝为B组和下列溶液反应,再取前面实验中得到的附有海绵状铜的4根铝丝洗净后作为C组和下列溶液反应作比较,实验现象记录如下:
| 热水 | 硫酸铜溶液(2.0mol/L) | 氯化铝热溶液(2.0mol/L) | 饱和氯化钠 热溶液 | |
| A | 只在开始时 有少量气泡 | 气泡较多,但比同浓度的氯化铜溶液少 | 有气泡, 比热水多 | 气泡比热水稍多,但比氯化铝溶液少 |
| B | 气泡比相应A多 | 气泡比相应A多 | 气泡比相应A多 | 气泡比相应A多 |
| C | 气泡比相应B多 | 气泡比相应B多 | 气泡比相应B多 | 气泡比相应B多 |
实验现象说明氢气的生成原因是多种因素作用的结果。试推测该同学原来的猜想有哪些(不一定填满,不够也可以自己添加):
(1)反应生成的铜和铝组成原电池促进铝和水反应;
(2) ▲ ;
(3) ▲ ;
(4) ▲ ;
(5) ▲ 。
查看习题详情和答案>>(2)在制备氢气的实验中,为加速锌与酸反应制取氢气的速率,也可以在酸中加少量_________溶液,或用_________与酸反应形成原电池加快反应速率。
(3)马口铁(镀锡铁)破损时与电解质溶液接触,_________先被腐蚀。
查看习题详情和答案>>(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解.写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式
(3)将铝片和镁片用导线相连,插入由A、D、E三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为
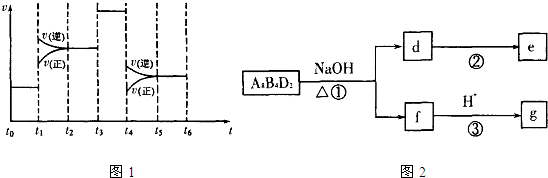
(4)化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),图1表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是
| 4 |
| a2 |
| 4 |
| a2 |
(5)化合物A8B4D2有如图2转化关系.其中,g是常用调味品的主要成分.写出反应①的化学方程式
| △ |
| △ |
设计实验方案完成d→e的转化