网址:http://m.1010jiajiao.com/timu_id_3837957[举报]
查看习题详情和答案>>
某有机物,它的蒸气密度是相同条件下空气密度的2.56倍。11.1g该有机物充分燃烧后的产物通过浓硫酸后增重8.1g,剩余气体通过足量澄清石灰水后生成45g白色沉淀。求:
(1)该有机物的分子式。
(2)该有机物有多种同分异构体,写出其中能水解的同分异构体的结构简式。
31.已知A为烃, B为烃的含氧衍生物. 由等物质的量的 A 和 B 组成的混合物 0.05 mol 在0.125 mol 的氧气中恰好完全燃烧, 生成 0.1 mol 的 CO2 和 0.1 mol H2O, 试通过计算回答下列问题:
(1)从分子式的角度看, 等物质的量A和B组成的混合物平均组成可用化学式表示为_________。
(2)另取一定量的A和B完全燃烧, 将其以任意物质的量比混合, 且物质的量之和一定,则:
①若耗氧量一定,则A和B的分子式分别为:
A ; B 。
②若生成的CO2和H2O的物质的量一定,则A和B的分子式为:
A ; B 。
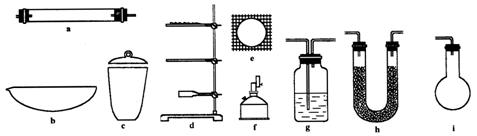
查看习题详情和答案>> 有机物的C、H含量常用燃烧和与CuO灼烧等方法使之生成![]() 和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器。
和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器。
(1)为确定某固体有机物的最简式(实验式)下述仪器中最少需要的种类有________种,它们是________,其中要一前一后用两次的是________,(填仪器编号)其作用前者为________;后者为________。但为完成测定还缺少的一种重要仪器名称是________。
(2)为确定固体有机物是烃还是其含氧衍生物,实验依据是________.
(3)为确定其分子式还需知道下述中的
A. 熔、沸点 B. 定温、定压下蒸气密度
C. 固定有机物的体积 D. 重要的化学性质
查看习题详情和答案>>