摘要:Cl2 KMnO4与浓盐酸 16HCl+2KMnO4=2KCl+2MnCl2+8H2O+5Cl2
网址:http://m.1010jiajiao.com/timu_id_3832542[举报]
KMnO4溶液与浓盐酸反应,可生成Cl2:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O.若生成71 g氯气,需参加反应的氯化氢为多少克?被氧化的氯化氢是多少克?
实验室以MnO2和浓盐酸反应制Cl2并净化和收集的装置如图所示,试回答以下问题: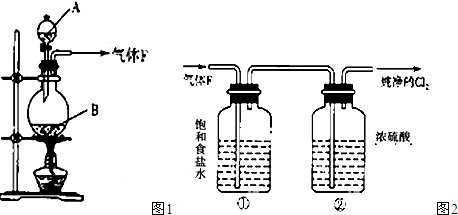
(1)如何检验装置的气密性?
(2)净化装置的顺序能否颠倒?为什么?
(3)以含14.6g HCl的浓盐酸与足量的MnO2充分反应,制得的Cl2在标准状况下总小于2.24L,原因可能是①
②
(4)据4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O;4HCl(g)+O2
2H2O+2Cl2;16HCl(浓)+2KMnO4═2KCl+2MnCl2+5Cl2↑+8H2O.判断MnO2、O2、KMnO4的氧化性由强到弱的顺序是
查看习题详情和答案>>

(1)如何检验装置的气密性?
(2)净化装置的顺序能否颠倒?为什么?
(3)以含14.6g HCl的浓盐酸与足量的MnO2充分反应,制得的Cl2在标准状况下总小于2.24L,原因可能是①
随着反应进行,盐酸浓度变小,MnO2与稀盐酸不反应,该反应停止
随着反应进行,盐酸浓度变小,MnO2与稀盐酸不反应,该反应停止
;②
加热过快,部分HCl挥发
加热过快,部分HCl挥发
.(4)据4HCl(浓)+MnO2
| ||
| ||
| 400℃~500℃ |
KMnO4>MnO2>O2
KMnO4>MnO2>O2
.实验室用KMnO4溶液与浓盐酸反应制取氯气.反应方程式如下:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
求:15.8g KMnO4参与反应时,产生的Cl2在标准状况下的体积为多少?反应中被氧化的盐酸的物质的量是多少?
查看习题详情和答案>>
求:15.8g KMnO4参与反应时,产生的Cl2在标准状况下的体积为多少?反应中被氧化的盐酸的物质的量是多少?
 如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题:
如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题: 如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题:
如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题: